при р. makrogeterotsiklich. пигменти. порфин молекула, съдържаща една линия (формула I). Формално получен от porphin чрез заместване на Н атома в цикъла на декември орг. радикали. Чрез AP включва такива важни пигменти като хемо-глобин, хлорофили. цитохроми и nek- др. ензими (каталаза, пероксидаза). AP също се намира в секретите на животни, птичи пера, черупки от яйца, черупки от мекотели, масла, битум, минерален орг. остатъци метеорити.
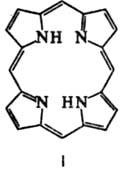
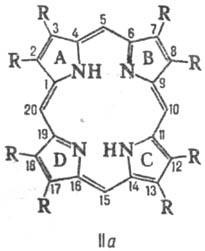
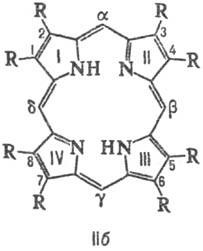
C. P. Атомите са номерирани съгласно IUPAC но menklaturam (формула Па) или Fisher (III). Четири атом C (5, 10, 15 и 20 на формула III) свързване на пиролови пръстени се нарича. мезо-въглеродни атома семейство.
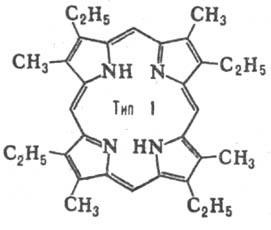
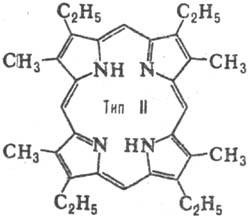
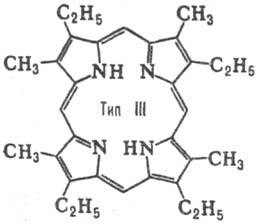
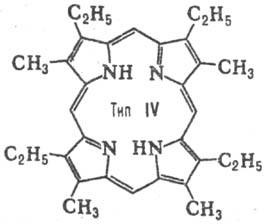
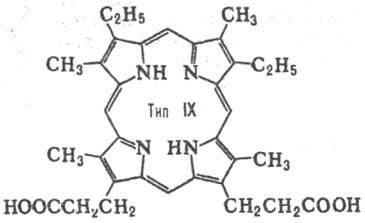
Брой на позиция изомери за P. определен брой-TION на заместници и тяхното подреждане в молекулата. За P. два заместителя (напр. СН3 и С2 Н 5), при условие, че и двата заместителя са налични във всяка от пироловия пръстен има 4 вида изомери. Когато има три декември Заместваща няколко вида увеличава до 15. П. Natural с два заместителя, притежават Ch. Пр. местоположение тип III, тип три-IX (виж. таблица.).
Порфин и AP-горещо стопен интензивно оцветени Кънектикът. (Глава Пр тъмночервен цвят ..); т разл.. порфин 360 ° С, P.-ok. 500 ° С. P. добра разтворимост. в СНС13. DMF, лошо в етанол и метанол, не зол. във водата. PA молекула са плоски и обикновено са свързани поради образуването на водородни връзки. Ултравиолетовият спектър на PI л макс
400 нм (m. Наречен. Soret лента, 400 д 000), 500 600 нм (е 15,000 или по-малко)
AP-ароматен. структура; притежават висока конюгиране енергия (840 кДж / мол), което се проявява в стабилността на съединенията. За порфирин цикъл се характеризира с наличието на две тавтомерни форми:
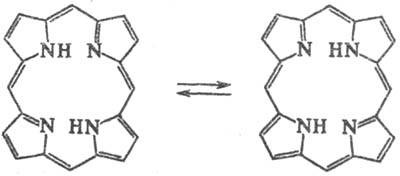
AP-амфотерен Conn. N атома в молекулата могат да придават протони за образуване на моно- или ново предикати, двете групи NH-протони разцепени за образуване на моно- или дианиони: RN 2porfirin, P 2- -dianion, P. -dikation слаби до ви; рКа 1 и рКа 2 (за етиопорфирин) 16, рК 3 oktaalkilporfirinov прибл. 5.5 (2.5% воден разтвор на RR додецил Na).
При взаимодействието. PP с метални соли да образуват метални порфирини naib. важна от които хем-порфирин или ferroproto (виж хемоглобин.); Naib. важно хидрогенирано. метало-порфирин -hlorofill. Металопорфирини лесно претърпяват р-ТА електрофил. заместване, гл. Пр. в мезо-позиция. За свободен P. тези р-ТА затруднено поради образуването в кисела среда дикатион без да влиза в електрофил. р-ТА.
PA и техните метални комплекси лесно се редуцират. Най-лесният начин за електрохимични потоци. редукция с образуване на моно- и дианиони, притежавани до силни и добре kleofilami реагира бързо (Ch. ARR. от Nym мезо-въглеродни атома) с протонни донори и електрофили като СН 3 I. Леко цикъл хидрогениране води P. на хлор (формула III) и Florin (IV), дълбоко-bacteriochlorin до (V), porfodimetenam (VI), porfomete-ни (VII) и porfirinogenam (VIII).
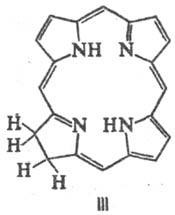
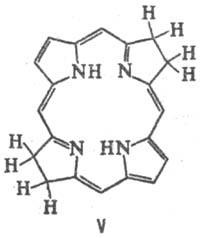
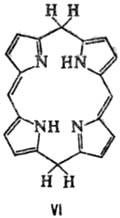
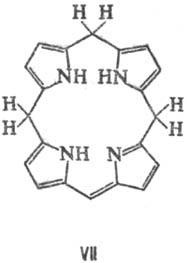
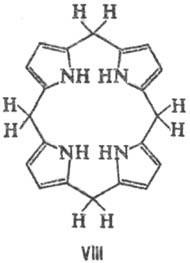
Ако е ненаситен, настоящето БКП. заместители, напр. VJ nilnaya група, за Conn porfirinogenov такива. възстановени амалгама Na. Обработка porfirinogenov O 2 Air светлина, йод или 2,3-дихлоро-5,6-ditsianoben-zohinonom ги кара да премине в P. Под действието на HI обикновено се случва, разликата на пръстена и образуване на пироли P. смес.
Под действието на мека или електрохимично окисляване стр и техните продукти на окисление метална форма катийонна радикали под въздействието на силни оксиданти (например SrO3 КМПО4 ..) има пръстеновиден процеп:
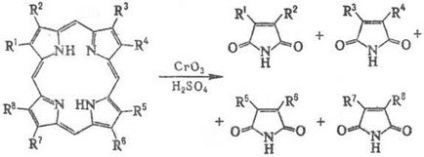
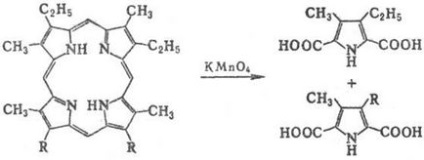
Окиси. разцепване на PG в организма води до образуването на жлъчни пигменти. P. относително лесно метилиран атоми на N, напр.
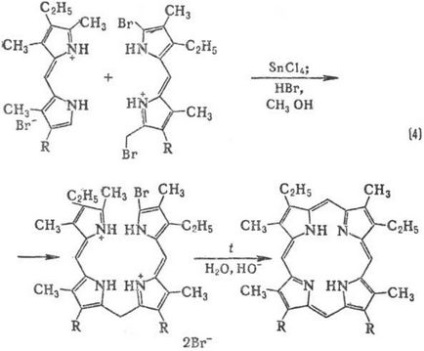
Метилови групи изпитват пространства. трудности в резултат макро цикъл е "велпапе". Методи за синтез monopirrolov P. кондензация с алдехиди (р-ционни 1); автокондензация monopirrolov съдържаща група в позиция 2 СН 2 X, където X = О Ac, OH, CI, Br, N (CH3) 2 (р-ТА 2); dipirrilmetenov кондензация и dipir-rilmetanov (3a и 3b); кондензация на tetrapyrrole Inger-медиация, притежавани до т. б. получен в ред от dipirrilmetenov, dipirrilmetanov или етапи на синтез monopirrolov (напр. р-ТА 4).
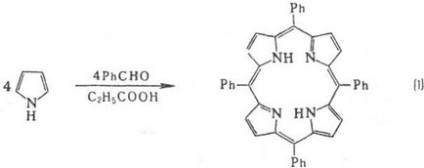
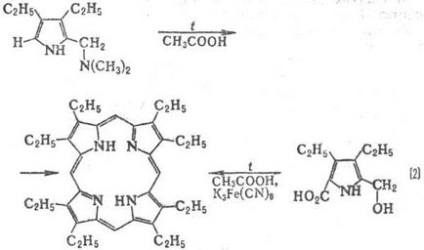
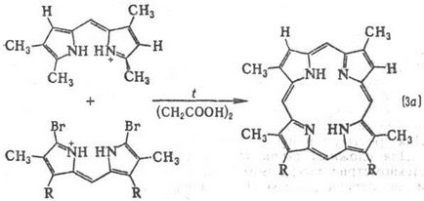
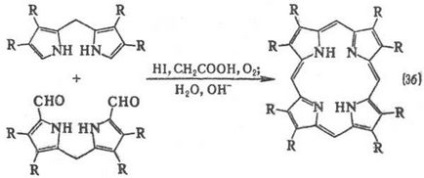
Клетките на растителни и животински организми P. биосинтеза е от глицин и янтарна до вас.
P.- основа на определена при р. багрила, модел Comm. за изследване на процеса на окисление на фотосинтеза, лек. лекарства при лечение на рак (например, хематопорфирин димер фото-Фрина.); AP-метални комплекси и окислителни катализатори епоксидиране на въглеводороди.
Лит. Chemistry биологично активни природни съединения, изд. NA Преображенски и RP Evstigneeva, М. 1976, стр. 100-84; Общо органичната химия. на. от английски език. Vol. 8, М. 1985, стр. 388-413; Порфирините: структурата, свойствата, Synthesis, Ed. NS Enikolopyana, М. 1985; Порфирините: спектроскопия. електрохимията, приложение, изд. NS Enikolopyana, М. 1987; Falk Й. Д. Порфирините и мета! Lopcrphyrins, Amst.-L.-N. Y. 1964; Делфини D. (изд.), Порфирини. Структура и синтез, с. 1, т А, L.-N. Y. 1978 P. P. Yevstigneyeva.
Химическа енциклопедия. - М. съветски енциклопедия. Ед. IL Knunyants. 1988 година.
Свързани статии
