# 132; Не беше обичайно явление море сияние. Monster, поп-в повърхностните водни слоеве, да починат няколко toise на морското равнище, както и от това дойде светъл, лек необяснима сила, която се споменава в докладите на много капитани # 133;.
- Да, това е просто една група от фосфоресциращи организми! - каза един от служителите.
- Вие сте прав, сър, - казах твърдо. - никога не Foladi или салпа не излъчва такъв светлинен вещество. Тази електрическа светлина произход # 133; # 147;
Фиг. 1. Получаване на електричество в ТЕЦ
Кои са читателите на едно дете не потъват в дълбокия океан, за да # 132; Nautilus # 147;? Ток за капитан му Немо получена чрез директно превръщане на химическа енергия в електричество в натриева амалгама батерия. Сега голяма част от електроенергията се издава чрез преобразуване на химическа енергия чрез окислително-редукционни реакции. На окислител е кислород, въздух и редуктор (горивото) - .. въглища, природен газ, масло и др Разликата между изходните продукти и енергийни вещества се превръща в топлина, и след това в механично движение, и - в електричество. За изпълнение на тази схема трансформации, необходими сложни, обемисти и скъпи мерки - котли, турбини, генератори, и в хода на тези трансформации голяма Енергията, освободена половината загубени.
Разглеждане на реакцията на редокси (първата връзка във веригата на трансформации) показва дали електрона съблазни се с окислителя молекули в молекулите на горивото чрез проводник, и така се превръща директно в електрическа енергия на реакцията не може да бъде? За първи път той е дошъл да съди главата и английски аматьорски учен Сър Уилям Гроув преди 165 години. Неговата единица е представена от електрохимичната клетка, анодът е окислен с водороден на катода за намаляване на кислород и жица свързва анода към катода, токът продължи. Сър Grove нарича вашата машина # 132; газ батерия # 147; и името # 132, # 147 горивни клетки; това устройство е получил петдесет години по-късно, с лека ръка на Лудвиг Mond (също любител химик, в основното и съща професия - бизнесмен, един от основателите на огромния # 132; Imperial Chemical Industries # 147).
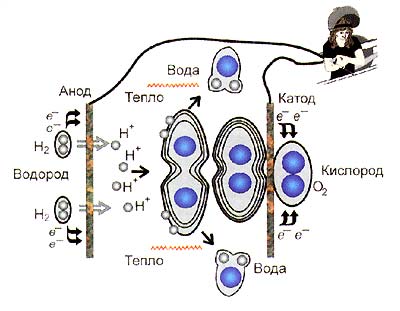
Фиг. 2. Директно преобразуване на химическа енергия за електрическо поле енергия в редокс реакция
При работа, почти не се нагрява горивния елемент - се освобождава в хода на енергия реакция се превръща директно в електричество. Тъй като не горивен елемент трансформира посочено междинно химично енергия в топлина, неговата ефективност не се ограничава до правило Карно и в зависимост от конкретната реакция, и може да бъде 100%, и дори повече! Разбира се, # 132; производство на енергия от нищото # 147; Това не се случи, но в някои случаи се дължи на промяна в реакцията не само енергия, но също така и ентропията на реагентите на енергийните параметри на електрическото поле и преминава част от топлинната енергия на околната среда. Днес апарат Grove - е тънка (1-3 mm) правоъгълна кутия, която съдържа два електрода и концентрира луга - електролит.
Анодът и катодът - е страничната стена, и те са съответно подава кислород и водород. Електродите осигуряват контакт газ и електролит, тяхното подреждане е показан в дясно. Charge прехвърляне се извършва в границата от три фази - електрода, газът и електролит: електрона преминава от водород за въглища частиците и молекула водород разделя на протони, които реагират с хидроксилните молекули:-
2Н2 + 4ON - → 4H2 О + 4е -.
-
В O2 + 2Н2 О + 4 е - → 4ON -.
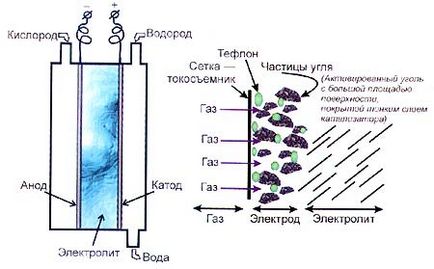
Фиг. 3. горивната клетка кислород водород с алкален електролит, за дифузия на газ електрод за него
Това е основният проблем: реакцията на окисляване (горене) на гориво са при стайна температура бавно - реагира в значителна част от сместа от молекули, необходими за стотици години. Горивният елемент е обвито много ниска плътност на мощността, и тя трябва да има огромна размер.
Необходимо е да се ускори катодна и анодна реакция, която може или да се използва катализатор, или повишаване на температурата на клетката. В случай на кислород водород клетка с алкален електролит, добър избор на катализатор оказа възможно; Най-добрият катализатор за двата електрода - платина тънък слой, който покрива електродите. Тези елементи на горивото са били толкова успешни, че те са били използвани през 60-те години на миналия век, за да предоставят на енергията на експедициите до Луната (разработчик на горивни клетки за лунната експедиция е сър Франсис T. Бейкън, пряк потомък на известния философ и държавник Франсис Бейкън).
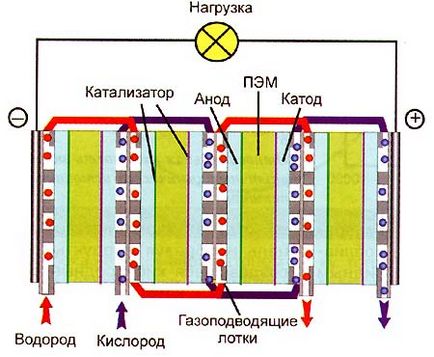
Фиг. 4. верига водород кислород горивната клетка с ТЕМ (батерия)
Сега, като # 132, # 147 на електролита; филм се използва - полимерен електролит мембрана (ПОМ). Тя се състои от големи молекули поливалентна киселина, в която страничната верига въглероден скелет на групите остатък на приложените [-SO3]. и протоните се движат свободно в полимера. Най-често срещаният ТЕМ # 151; от поли [тетрафлуоретилен] -perftorsulfonovoy поликиселини известни под търговското наименование # 132; Nafion # 147. Modern горивен елемент се състои от тънък (50 микрона до 250 микрона) филм # 132; # Nafion 147, с две катализаторни покритие страни (анодни и катодни); за слоевете са пресовани срещу катализаторни плочи - токоприемника направен от всякакъв (може да има разлики между най-добрите варианти) на порестия газопропусклив материал, провеждане на ток добре. Към плаките, на свой ред, пресовани тави с канали, чрез които се доставят на катода и анода и водород кислород. Обикновено, при максимална мощност клетка напрежение е 0.5-0.6.
След преодоляване на техническа пречка за разработчици роза икономическата: кислород-водород се оказа много скъп елемент в производството и в режим на работа (за мисии до Луната това може да бъде пренебрегната). Висока стойност на горивния елемент предизвика прилагането на платина и полимер електролита, е също скъпа и сложността на производствени техники.

Фиг. 5. мощност на батерията от 500 W от елементите
Естествено предлагат два начина за намаляване на оперативните разходи: замяната на водородно гориво от обичайното (.. метилов алкохол, дизелово гориво и т.н.) или намаляване на газ за изискванията за чистота. За решаването на последните (очевидни леки) задачи разработчиците използват като електролит 100% фосфорна киселина и температурата се повишава до елемент 150-200 ° С, което води до относителна успеха - стана възможно да се приложи технически водород, съдържащ 12% въглероден монооксид , В момента работа, няколко клетки с опит такъв дизайн, мощност от 5 кВт до 200 кВт. Фосфат клетка алкална гориво по-евтино, но не толкова ефективен (ефективност 40-50%), и все още твърде скъпи (около $ 500. / KW). Операция при по-високи температури го прави неподходящ за захранване преносими електроника и нуждата от отопление, преди започване на границите на приложение за транспортиране (това се отнася за всички от следните елементи именувани с отопление).
В още по-високи температури (800-1000 ° С), работещи на горивната клетка с твърд електролит оксид. Има не катализатор елемент се състои от тънък смес от итрий и циркониев оксид слой - оксид електролита с висока мобилност на свободните места на кислородни йони твърдо вещество; от двете страни на електролита са решетка - токоприемник. От страна на анода гориво реагира с йони O 2- решетка, като електроните на външната верига и формиране реакционни продукти; Създадена кислородни свободни да се движат към катод слой на електролита, докато електроните - към катода през външна верига, производство на електрически ток. На катода, кислород отдава електрони и йони O 2 запълване идва за свободните работни места на катод кислород. Такъв елемент има горивна ефективност на над 50% не съдържа платина, и горивото може не само служи за това водород и природен газ, но дори и дизелово гориво. Проблемът е наличието на високо-температурна зона, което изисква използването на скъпи материали на конструкцията и помощни единици; експлоатационния живот на горивните клетки е достатъчно все още не е голям. Подобно на горивните елементи на разтопен карбонат горивните елементи с твърд електролит оксид ще бъдат най-подходящи за използване в големи стационарни инсталации.
Така че, въпреки забележителния напредък в областта на горивните клетки от времето на експедицията до Луната, енергията им остава все още твърде скъпи за широко използване - ако случаят стигне до предлагане на жилища, предприятия и превозни средства. Ето един прост пример: цената на най-готови за търговска употреба, фосфат горивни клетки, като се вземе предвид времето за амортизация, това води до увеличаване на разходите от 1 киловатчас енергия за 10 рубли. Разходоефективността на водород при около 50% на елемента дава разход на енергия е не по-ниска от 30 рубли за киловатчас, както и това, без да се има предвид всички възможни режийни разходи. А цената на дребно # 132, # 147 нормално; електроенергия в Америка е по-малко от 20 цента, което е около пет рубли за киловатчас.
Фиг. 6. относителната енергийна плътност от различни източници на химическата енергия на
За да водородни горивни клетки се превърна в конкурент на топлинни и атомни електроцентрали, енергията, която трябва да падне в цената най-малко веднъж от осем, с по-евтин искал самия елемент, какво друго може да се очаква, и водород - за които няма видима причина.
Фиг. 6 показва, че използването на горивни клетки за преносими електроника революция обещания - увеличаване период на непрекъсната работа на автономни електронни устройства 10-20. Освен това, на всички видове горивни клетки е най-добрият кандидат клетка само с TEM: други изискват високи температури за труд и спомагателни устройства (например помпи.). Трудно е да си представим, че успяват да побере преносим захранващ източник с загрява до 200 ° С с фосфорна киселина и помпа за въздух, помпа. И който иска да го купи?
Фиг. 7. енергийна плътност на водороден газ, течен водород, литиево-йонни батерии и метанол
Защо всички преносими електроника продължават да вървят в батерии и акумулатори, които не са горивната клетка с PEM? Причината е проста: - в който се използва газообразен водород, който има високо енергийно капацитет на единица тегло, но много ниска - за единица обем, тъй като тя е газ. Както се вижда от фиг. 7 за постигане на същата обемна енергийна плътност като тази на литиева батерия, е необходимо да се компресира на водорода 72 атм, и като се отчита обемът на елемент балон и - до 100 атм.
Не е изненадващо, че източници на енергия за преносими електроника, които консумират водород, не са много атрактивни за купувачите (пример на такъв източник е показано на фиг. 8).
метод # 132; сгъстяване # 147; Това може да стане втечняването на водород са необходими, но това прави метода на температурата не е приложим за преносими устройства. алтернатива # 132; сгъстяване # 147; водород - използването на гориво. Тя трябва да има висока енергийна плътност, за да бъде евтино и безопасно (безвреден. Не е много токсичен, не е взривоопасен, не запалим при контакт с въздух или вода и други подобни. Г.). Тъй като горивният елемент - електрохимична система, желателно е, че повече гориво и добре се разтваря във вода. По-добре отговаря на всички изисквания на метанол - това е евтин, се смесва с вода във всякакви пропорции, лесно се разгражда при лечение вода и има два пъти по-висока обемна плътност на енергията от дори течен водород.

Фиг. 8. горивна клетка мощност 50W POE Захранването за електронни преносими устройства
Тя може да се види, че катода на елементите на двете е един и същ и цялостния дизайн също е сходен. Разликата се състои в това, че в анодното отделение на една клетка се подава газообразен водород и реакцията протича-
Н2 → 2Н + + 2е -,
-
СН3ОН + Н2 О → СО2 + 6Н + + 6e -.
Фиг. 9. Сравнение на принципа на работа на клетките на метанол и водород гориво с полимерен електролит: горната част на ръката верига е метанол ТЕМ елемент, по-ниската # 132; ръкав # 147; - водород ТЕМ елемент
Но ако катализаторът (платина) се избира за първата реакция. това позволява да се ускори и да получат елемент с плътност на мощността от около 0.5-0.7 w / см 2 търсенето на втората реакция, катализаторът е по-трудно - метанол до клетъчна плътност добра мощност ТЕМ на проби 0.02-0.03 W / cm 2. Тези стойности на ниска плътност на мощността води до факта, че консумацията на енергия за осигуряване на типичен преносимо устройство (10-30 W) на електрода на горивна клетка трябва да бъде прекалено голяма. Така, например, че горивният елемент, хранене преносим компютър, трябва да сте електроди, с площ от около 500 cm 2 и горивната клетка ще бъде по-голям от компютъра. Цената и казват нищо - само една част от катализатор покритие полимерен електролит размер филм 600 cm 2 ще струва повече от $ 100 - $ 1000 вече около ..
Проблемът произтича от механизма за катализатор многостепенен електронен трансфер по време на окисляване дори такива прости органични молекули като метанол.
Фиг. 10 показва, че метанолът се адсорбира молекула на първия електрод, след това, по време на окислението, един след друг губи протони, и се превръща в силно адсорбирания карбонил група, която не желае всеки десорбира или окислява допълнително.
Фиг. 10. стъпаловидно механизъм електронен трансфер през електроокислението метанол върху платинов
В резултат само за две минути след началото на окисление на електрод платина отровен твърдо адсорбира и карбонилни групи не могат да катализират окисляването на метанол.
Опитите да се намери катализатор, който се съсредоточава върху активен окислен като метанол и въглероден окис, като ще доведе до решаване на проблема - имаше катализатор Pt / Ru-сплав. Рутений карбонилни групи окисляват добри, но - лошо катализатор за окисление на метанол, платината окислява метанол, но заразени с въглероден окис. Pt / Ru-сплав - твърд разтвор, повърхността на който се състои от платина и рутений атома. Създадена на карбонилната група на платина атома мигрират към съседен атом рутений, където окислява.
Но производството на катализатор на микро ниво не съществуват перфектни смесване на атоми на платинени и рутений атомите на всеки елемент са привлечени от атомите на рода си, събрани в съцветия, и механизмът работи само по въпросите на миграцията в рамките на тези клъстери. Необходимо е или да се измисли нов катализатор за окисление на метанол във въглероден монооксид нечувствителен, подобряване на смесване или платина и рутений атома в Pt / Ru катализатор (наскоро отбеляза 30 години на изобретението си). Сравнение патентовани методи за получаване на Pt / Ru катализатор и патенти, посветени на други катализатори за метанол ПОМ горивна клетка, това показва, идея, която подобрение Pt / Ru катализатор е по-популярни. Основните идеи в тази област - като прави възможно по-малък Pt / Ru сплави клъстери на субстрати на въглеродни материали с огромна повърхност; вече получен окуражаващи резултати с използване на въглеродни нанотръби. Но докато въглеродни наноматериали скъпо платина и рутений.
Нека се опитаме да се оцени vozeystvuet като появата на нов продукт на развитието на цивилизацията. На първо място е източник на силовата електроника стимулира допълнително вникване в ежедневието. Възможност за работа с компютър, където и да е, без да се налага да се притеснявате за наличието на близкия електрически контакт, ще доведе до увеличаване на продажбите на преносими компютри и намаляване на продажбите на работния плот. Ще се разпространи думата широко книги - специализирана мини-компютри, предназначени за четене на текст. Това ще доведе до преминаването на големите издатели за производство на книги, посветени на CD- и DVD-медии; разширяване на пазара на преносими телевизори с плосък екран и DVD-плеъри и др. г.
Членове-близкия обект:
Пробив в водород бъдеще. Е. Glebov.
Стъпки за свръхлеки власт. SM Комаров.
Palladium. VV Blagutin.
Твърди полимерни електролити. AM Тимонов.
Твърди оксид електролити. А. Demin.
Пет истории за nanocarbon. Корнилов M. Yu.
Размисли за някои енергийни въпроси. AE Sheyndlin.
Ще има ли революция в енергетиката? Николаев.
Синтетичен лотосов лист. А. Hachoyan.
