Физика за всички
Наличието на "neotnimaemoy" при абсолютната нула енергия не е специален собственост на хелий. Оказва се, че на "нула" енергията на разположение за всички вещества. Само хелий тази енергия е достатъчно, за да се предотврати атомите образуват редовно кристална решетка.
Не мислете, че хелий не може да бъде във вид на кристал. необходимо за кристализиране на хелий само повишаване на налягането до около 25 атм. Охлаждането се извършва над този натиск ще доведе до образуването на кристално твърдо вещество с изцяло конвенционални хелий свойства. Хелий образува лице центрирана кубична решетка.
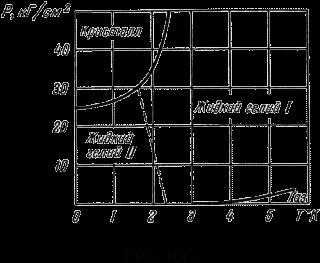
Фиг. 106 показва схема на хелий. Той е много различен от всички други вещества, диаграми нямат тройната точка. Топене и кипене криви не се пресичат.

Какво решение
Ако бульон със сол и се разбърква с лъжица, а след това няма да има следи от сол. Не бива да мислим, че солта зърна просто не се виждат с невъоръжено око. Кристали на сол по никакъв начин не могат да бъдат открити поради това, че те се разтварят. Ако podbavit в пипер бульон, решението няма да работи. Можете дори да се смесват бульона в продължение на дни - малки черни точици изчезват.
Но това означава, че - "решение вещество"? В крайна сметка, атоми или молекули, от които е изградена, не могат да бъдат бездната без следа? Не, разбира се, че не изчезнат. След разтваряне изчезва само петно вещество кристал, концентрацията на молекулите на един вид. След разтваряне се разбъркване на смес от частици, при които молекулите на едно вещество, разпределени между различни молекули. Разтворът - смес от молекули или атоми на различни вещества.
Разтворът може да съдържа различни количества от разтворено вещество. Състав на разтвора се характеризира с концентрация, например, съотношението на броя на грам от разтвореното вещество на броя на литра разтвор.
Тъй като добавянето на увеличенията на разтвореното вещество разтвор концентрация, но не и за неопределено време. Рано или късно, решението да се насити и спира да "вземе" разтворител. Концентрацията на наситен разтвор, т.е. "Странична" концентриране на разтвора, наречен разтворимост.
Изненадващо много захар може да се разтваря в гореща вода. При температура 80 ° С в пълна чаша вода ще никакъв остатък 720 грама на захар. Това наситен разтвор е дебела и вискозен, готви го наричат захарен сироп. Ние сме доведе до цифрата за захар чаша сушилня на пране, с капацитет от 0,2 литра. Следователно, концентрацията на захар във вода при 80 ° С равна на 3600 гр / л (следва: "грама на литър").
Захар и сол са лесно разтворими във вода. Но нафталин във вода практически неразтворим. Различни вещества в различни разтворители разтварят напълно различни.
Разтворът се използва за отглеждане на монокристали. Ако окачени в наситен разтвор на малък кристал от разтворено вещество, изпаряването на разтворителя като разтворено вещество ще се приземи на повърхността на кристалите. В този случай, молекулата ще следва строг ред и като резултат от малък кристал превърне в голяма, останалия единствен кристал.
Разтвори на течности и газове
Възможно ли е да се разтвори на течността в течност? Разбира се, че можеш. Например, водка - е алкохолен разтвор във вода (или, при желание, вода, алкохол, - търсене в повече). Водка - един истински разтвор, водните молекули и алкохол напълно смесени в нея.
Въпреки това, не винаги чрез смесване на две течности получите този резултат.
Опитайте се да излее вода керосин. Да не се смесват няма да може да се получи хомогенна смес, тя е също толкова безнадеждно, че да се разтвори пипер в супата. След разбъркването се спира, течността в слоя: тежка вода - в долната част, по-лек керосина - в горната част. Керосин с вода и алкохол с вода - система за противопоставяне на разтворимост.
Въпреки това, има междинни случаи. Ако смесите въздух с вода, след това можем да видим ясно в съда два слоя. На пръв поглед може да изглежда, че на върха на въздуха и под водата. В действителност, и по-ниската и горния слой са разтвори: в долната част - водата, където разтваря част естер (концентрация от 25 г естер на литър вода), и най-добре - естер, който има значително количество вода (60 г / л).
Сега pointeresuemsya разтвори газове. Ясно е, че всички газове се разтварят един в друг в неограничени количества. Две газ винаги се смесват така, че молекулите проникват между молекулите един на друг. Наистина, няколко газови молекули взаимодействат един с друг, и всеки газ се държи в присъствието на друг газ, в известен смисъл, не се обръща "внимание" на партньора си.
Газове може разтварят в течности. Въпреки това, не е в количество, и в ограничен, не се различава в това отношение от твърдите вещества. В този случай, различни газове се разтварят по различни начини, и тези разлики могат да бъдат много големи. Водата може да се разтвори големи количества амоняк (в половин чаша студена вода - около 100 г), големи количества сероводород и въглероден диоксид. Малкото количество кислород е разтворим във вода и азот (0.07 и 0.03 гр на литър студена вода). Така, в един литър студена вода е само около една стотна от грам въздух. Все пак, това малко количество играе голяма роля в живота на Земята - в действителност, разтворен във вода кислород във въздуха дишане рибата.
Най-голямо налягане на газа, толкова повече тя ще се разтвори в течността. Ако количеството на разтворен газ не е много голяма, налягането между него и газ има пряка пропорционалност над повърхността на течността.
Кой не се радва на студено газирана вода, толкова добро питие жажда! Получаване на газирана вода е възможно поради зависимостта на разтворен газ под налягане. Въглероден диоксид се задвижва под налягане във вода (цилиндри, които са всеки терминал, който продава газирана вода). Когато водата се излива в чаша, налягането пада до атмосферното налягане и водата извлича "допълнително" газ под формата на мехурчета.
Като се има предвид тези ефекти, водолазите не може да бъде бързо, повдигнати от водата на повърхността. Под високо налягане в дълбочината на водолаза в кръвта разтваря допълнително количество въздух. При повишаване на пада на налягането, въздухът започва да се разделят като мехурчета и могат да блокират кръвоносните съдове.
В живота, думата "решение" се прилага към течността. Въпреки това, има твърди смеси, атоми или молекули се смесват хомогенно. Но как да получите най-солидни решения? С помощта на хаванче с чукало, няма да ги вземем. Следователно смесват вещества трябва първо да течност, т.е. стопени, след това смесване на течността и сместа се оставя да се втвърди. Можете да го направите още нещо - да се разтвори двете вещества, които искаме да се смесват в течността, а след това да се изпари разтворителя. Такива методи могат да се окажат по-твърди разтвори. Може да получите, но обикновено не може да се получи. Твърдите разтвори - е рядкост. Ако солена вода, за да изхвърлите парче захар, то е напълно разтворен. Изпарява вода; се показват в долната част на чаша фини кристали от сол и захар. Сол и захар не осигуряват твърди разтвори.
Тя може да се разтопи в тигел, кадмий и бисмут. След охлаждане, ще видим в микроскоп смес от кристали на бисмут и кадмий. Бисмут и кадмий също не образуват твърди разтвори.
Необходимо е, че не е достатъчно условие за появата на твърди разтвори е близостта на молекули или атоми на смесване вещества по форма и размер. В този случай, един вид на кристали, образувани по време на замразяване на сместа. Възлите на всяка кристална решетка обикновено случайно населените атоми (молекули) на различни класове.
Свързани статии
