Урок Относно: Протеини
актуализиране на знанията за протеините на курса по биология;
за изследване на физичните и химичните свойства, цвят реакциите на протеини;
студентите трябва да могат да се характеризират състава и структурата на протеините,
функцията на протеини в клетката, тяхната стойност за цял живот.
Оборудване и реактиви: концентрира HNO3. протеин, разтвор CuSO4. NaOH, алкохол лампа, кибрит, притежател тръба.
Протеини, според Енгелс, форма на съществуване на живот.
"Навсякъде, където животът ни е свързана с никакви протеин на тялото, и навсякъде, където се срещаме всеки протеин на тялото, а не да са в процес на разлагане, без изключение, се сблъскваме с феномена на живота." (Marx, Engels. Събрани строителство. Т. 20). Протеин - строителен материал, работи двигателя, каталитична, транспорт, безопасност, енергия функция.
Протеините бяха изолирани в отделен клас биологични молекули в XVIII век в резултат на работата на френски химик Antoine Fourcroy и други учени, в които се наблюдава свойства на протеини коагулират (Денатуриране) под въздействието на топлина или киселини. По това време се изследва протеини като албумин ( "белтък"), фибрин (протеин от кръвта) и от пшеничен глутен.
В 80-те години на руския биохимик на XIX век Danilevsky АЙ малко по-късно - (1903 грама) немски учен Е. Fisher - полипептид напреднали теория на структурата на протеини: протеини верига от остатъците # 945; - амино киселини чрез пептидни връзки # 8213; CO # 8213; NH # 8213;.
Сега е известно, 22 аминокиселини, които създават безброй протеинови молекули. Всеки от които има собствена, добре дефинирана, редът на промяната на аминокиселината. Има четири структури на молекулата на протеина. Основни - редуващи се остатъци # 945; - аминокиселини; вторичен - верига усукани в спирала; третичен - конфигурация, който взема пространство навита спирала (осигурява биологичната активност на молекулата на протеин); Кватернерни - свързани една с друга макромолекулни протеини. При нагряване, разклащане унищожени третичната структура на протеина, той губи своята биологичен ефект.
Протеини - с високо молекулно тегло комплекс природни съединения, изградени от остатъците от # 945; - аминокиселини, свързани с пептидни връзки (амид) # 8213; CO # 8213; NH # 8213;.
Броят на аминокиселинни остатъци в рамките на протеиновата молекула, е различна: в инсулин 51 (20 в една и 31 - в други вериги) в миоглобин - 140. Молекулните тегла на протеините могат да варират от 10 000 до няколко милиона.
Г-н (яйчен протеин) = 36000; Н (мускулния протеин) = 1 500 000 Състав на хемоглобин се изразява с формула (C738 H1166 O208 N203 S2 Fe) 4. Изчислява неговото молекулно тегло е лесно.
Протеините са основният превозвач на живот. Информация за състава и структурата на протеините, получени при изследване на продуктите на хидролизата. Сега е установено, че молекулите на повечето протеини са съставени от 22 различен # 945; - аминокиселини.
протеини състава включват: С - 50 - 52%; N - 6, - 8%; О - 19 - 24%; N- 15-18% S- 0,5 - 2,0%.
Съвременните изследвания позволява да се разграничат протеиновата структура на първична, вторична, третична и четвъртична структура. (Slide 6).
Съгласно първичната структура на протеин се разбира, че точната последователност от позиция на отделните аминокиселинни остатъци в макромолекулата (всички ковалентни връзки, твърдо вещество). P.228 на учебника, Fig.37.
Вторичната структура - формата на полипептидна верига в пространството (често спирала). Протеин верига усукани в спирала (поради множество водородни връзки).
Третичната структура - реалната триизмерна конфигурация, която се проявява при завиване по спирала полипептидни вериги на протеини, настъпващи при дисулфид, водород и други връзки.
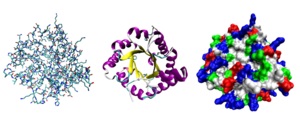
Различни начини за снимки на триизмерната структура на протеина.
На четвъртичната структура - връзката помежду макромолекули протеини. Образува комплекс. S.229, Fig.40.
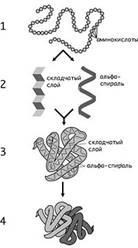
Нивата на протеинови структури: 1 - основната; 2 - средно; 3 - третичен; 4 - кватернерен.
Много протеини (глобуларни) разтворими във вода, разтвори на соли, киселини и почти всички разтворими в основи; не се разтварят в органични разтворители; неразтворими протеини (влакнести), от които конструираната тъкани на живи организми (кожата, сухожилията, мускулите, нокти, коса) и плазмените протеини са разтворими.
1) хидролиза (при нагряване с разтвори на киселини, основи, чрез действието на ензими)
H2N # 8213; СН2 # 8213; C # 8213;: N # 8213; СН # 8213; C # 8213;: N # 8213; СН # 8213; С = О → H2N # 8213; СН2 # 8213; С = О +
H2O СН2 H2O СН2ОН ОН
+ H2N # 8213; СН # 8213; С = О + H2N # 8213; СН # 8213; С = О
Хидролиза на протеини се редуцира до хидролиза на полипептидни връзки. Същото се намалява и усвояването на протеини:
Протеин аминокиселина ↔ → кръв към всички клетки и тъкани.
2) денатуриране - смущения на естествената структура на протеин (под действието на топлина и химикали)
денатуриране на протеина от кокоши яйца при висока температура
Свойства на __________ киселини
__________ свойства бази
4) цветни реакции на протеини - качествен отговор
Лаборатория опит. Правилник за работа!
а) ksantoproteinovaya реакция.
Излива се в епруветка малко протеин. ADJ него 3-4 капки концентрирана азотна киселина. Обърнете внимание на промените.
Протеин + HNO3 конц. → жълто оцветяване
б) взаимодействие на биурет.
Излива тръба малко натриев хидроксид, добавяйки към него разтвор на меден сулфат (II), така че остана алкален в излишък. Към този разтвор утайка прилив протеин. Имайте предвид, какво се е променило.
Протеин + Cu (OH) 2 ↓ → лилав разтвор.
Как иначе може да се определи протеин? (В горене - миризмата на изгорелите пера).
Заключение: Качеството на протеини взаимодействат с концентрирана азотна киселина (жълт цвят) с хидроксид прясно утаен мед (II) (виолетов разтвор) и горивни протеини (миризма изгорелите пера).
Сред органичните съединения, съдържащи се в жива клетка, решаваща роля играе протеини. На тях се падат около 50% от масата на клетките.
Протеините са градивните елементи на мембрани, органели и клетъчни мембрани. Тя е изградена на кръвоносните съдове, сухожилия, коса.
Те изпълняват каталитично функция. Всички клетъчни катализатори - протеини (ензимно активни центрове), структурата на активния център на структурата на ензим и субстрат точно съответстват един на друг.
Контрактилните протеини предизвикват движение.
Протеини изпълняват роля транспорт - хемоглобин в кръвта протеин пренася кислород и придава на всички тъкани.
Протеини служат защитна функция - производство на протеинови органи антитела за неутрализиране на чужди вещества.
При разлагане на 1 г протеин 17,6 кДж на енергия се освобождава. (Разлага протеини на СО2. NH3. Урея (NH2) 2, СО и Н2 О).
В мускулите, - до 80% в далака, кръвта, белите дробове - около 72% в кожата - 63% в черния дроб - 57% в мозъка - 15%, мастната тъкан, кост и зъб тъкан съдържа от 14 до 28% протеини ,
Протеините са част от много лекарства. Работата по изкуствен производство на протеини (синтезиран инсулин, рибонуклеаза).
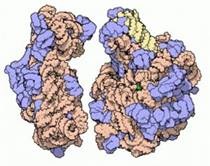
Молекулното модел на малки (вляво) и високи (вдясно) субединици на бактериалната рибозома - молекулярна машина, синтезиращи протеини. Синият цвят показва, протеините в рибозомата, но главната роля се играе от структурната рРНК.
Това е важно, тъй като експертите на Световната здравна организация смята, че около половината от населението на света е в състояние на протеин глад и недостиг свят на храната протеини е около 15 милиона. Тона годишно в размер на прием на протеини в възрастен на ден 115 грама.
Ние си спомни какво знаете за протеини от хода на биологията, изследва химичните свойства на протеини и тяхното значение в живота. Предлагам ви да проверите знанията си минало, за да отговаря на въпроси. Вие трябва да поставите на липсващите думи или фрази.
Основният превозвач на живота е ....
... - са сложни молекулни съединения, изградени от ....
Елементният състав на протеини: ....
Молекулното тегло на протеините варира от ... до ....
Много протеини са разтворими във ... почти всички разтворими във ....
Неразтворимите протеини, които са изградени ....
В структурата на протеина ... разграничи структура.
Функцията на протеини в тялото ....
протеини; салда # 945; - аминокиселини.
Десет хиляди, милиони.
Вода, солеви разтвори, киселини; основи.
Тъкан на живите организми: кожата, сухожилията, мускулите, ноктите, косата.
Първични, вторични, третични, четвъртични.
Строителство, каталитичен, мотор, транспорт, безопасност и енергетиката.
"5" - всички отговори са верни; "3" - 3 грешен отговор;
"4" - 1-2 грешни отговори; "2" - 4 или повече грешни отговори.
Протеини - с високо молекулно тегло комплекс природни съединения, изградени от остатъците от # 945; - аминокиселини, свързани с пептидни връзки (амид) # 8213; CO # 8213; NH # 8213;.
Броят на аминокиселинни остатъци в рамките на протеиновата молекула, е различна: инсулин - 51, миоглобин - 140. г (протеин) = 10 000 до няколко милиона.
Г-н (яйчен протеин) = 36000; Г-н (протеин в мускулите) = 1,5 милиона.
Основно - последователност от редуващи се аминокиселини (всички връзки ковалентни, твърдо вещество).
Средно - формата на полипептидната верига в пространството (предимно спирала). Протеин верига усукани в спирала (поради множество водородни връзки). Третичен - истински триизмерна конфигурация, която се в пространството на усукана спирала (чрез хидрофобни връзки), някои S - S - връзки (дисулфидна връзка).
Кватернерни - свързани една с друга макромолекулни протеини.
1) хидролиза (при нагряване с разтвори на киселини, основи, чрез действието на ензими)
H2N # 8213; СН2 # 8213; C # 8213;: N # 8213; СН # 8213; C # 8213;: N # 8213; СН # 8213; С = О → H2N # 8213; СН2 # 8213; С = О +
H2O СН2 H2O СН2ОН ОН
+ H2N # 8213; СН # 8213; С = О + H2N # 8213; СН # 8213; С = О
Хидролиза на протеини се редуцира до хидролиза на полипептидни връзки. Същото се намалява и усвояването на протеини:
протеин аминокиселина ↔ → кръв към всички клетки и тъкани.
2) денатуриране - смущения на естествената структура на протеин (под действието на топлина и химикали)
Свойства на __________ киселини
| __________ основни свойства
4) цветни реакции на протеини - качествен отговор
а) ksantoproteinovaya реакция.
Протеин + HNO3 конц. → жълто оцветяване
б) взаимодействие на биурет.
Протеин + Cu (OH) 2 ↓ → лилав разтвор.
в) горене - миризмата на изгорелите пера.
Заключение: Качеството на протеини взаимодействат с концентрирана азотна киселина (жълт цвят) с хидроксид прясно утаен мед (II) (виолетов разтвор) и горивни протеини (миризма изгорелите пера).
Ролята на протеини в клетката.
1. Строителен материал - образуване на обвивка, органели и клетъчни мембрани. Построени кръвоносните съдове, сухожилия, коса.
2. каталитично ролята на - всички клетъчни протеини катализатори.
3. двигателната функция - контрактилните протеини предизвикват движение.
4. Транспортна функция - кръвен протеин хемоглобин пренася кислород и придава на всички тъкани.
5. Защитно роля - производство на протеинови органи антитела за неутрализиране на чужди вещества.
6. Енергийна роля: един грам протеин → 17,6 кДж.
Свързани статии
