Химическа реакция се случва, когато се образуват едно комуникационно разрушаване и др. Производството на определена реакция зависи от няколко фактора, основните от които са природата на реагиращите молекули (реагентите) и атакуват реагенти, температура, концентрация на компоненти на катализатора. Значението да се определи механизма на реакцията принадлежи към естеството на частиците (междинни), които са оформени в междинни етапи на разделяне химична връзка.
Дисоциацията ковалентна връзка $ С-Х $ може да се появи в три основни схеми (фиг. 1).
Както се случва разцепване резултат хетеролитична връзка пълно изместване електронна двойка за конкретен атом за образуване на съответните въглеродни - йони или карбанионите карбокатиони. Хемолитична прекъсване връзки образуват свободни радикали.
Nature, образуването и стабилността на междинни частици
Органични йони и радикали са основните междинни съединения и по-голямата част от реакции, показващи значителна реактивност и действат като реагенти.
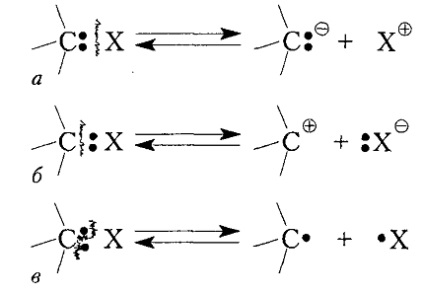
Фигура 1. дисоциация връзка $ С-Х $ с образуването на - карбанион, - един carbocation и - радикал; и б - хетеролитична (йонен), в - хемолитична (радикал) разделяне
карбокатиони
Карбокатиони имат положителен заряд ($ + I $) при въглероден атом, който е в състояние хибридизира. Следователно, структурата carbocation плоската и три хибридни орбитите са разположени в една равнина под ъгъл 120 $ ^ \ Circ $. Елитен $ р-AO $ е перпендикулярна на тази равнина.
Образуването на карбокатиони. Съществуват няколко метода за образуване на карбокатиони. Основните от тях са:
- протон присъединяване на някои съединения, включително главно да бъдат споменати, ненаситени въглеводороди и алкохоли.
- Директен йонизация полярен връзка $ С-Х $ под действието на външната среда. Такова дисоциация освен тяхната полярност връзка улеснява от присъствието на полярен разтворител, или катализатор, например киселина на Люис
- В каталитична изомеризация на алкани и под действието на алкани superacids като комплекс флуоросулфонова киселина - pentaftoroantimonat.
стабилност на карбокатиони
Известно е, че енергията хетеролитична разцепването на $ С-Х $ за образуване на carbocation (фиг. 1, б) е достатъчно висока и в газова фаза е, например, алкани, 900-1300 кДж / мол. В резултат на това са нестабилни карбокатиони, имат значително реактивност. стабилност Carbocation е по-висока, толкова по-делокализираният положителен заряд. Алкилови заместители стабилизиране на донора carbocation неговите свойства, да помогне за намаляване на електронен дефицит при въглероден атом с положителен заряд. Заместителите с отрицателен $ I ^ - $ дестабилизиращ ефект carbocation, и тя става по-нестабилно.
Решете контрол по всички предмети. 10 години опит! Цена от 100 рубли. период от 1 ден!
Въпреки това, индукционни и giperkonyugatsionnye ефекти на на показват относително слаба стабилизиращи фактори карбокатиони, освен този ефект до голяма степен се възстановява след като премахнете депутат от свободен $ р-AO $. Най-голямо влияние върху стабилността на карбокатиони произвежда мезомерен ефект на ненаситени връзки чрез конюгиране свободен $ р-AO $ с $ \ пи $ -връзките, разположен в $ \ алфа $-позиция, за да орбитите
Стабилизиране карбокатиони, могат да се извършват също чрез конюгиране освободи $ р-AO $ carbocationic център с неразделен електронна двойка на хетероатом ($ р-р $ долепени):
Фигура 2. Стабилност на алкилови радикали
До голяма степен върху стабилността на карбокатиони засяга разтворител. полярен медии катион може да съществува в свободно състояние в резултат на реакцията на хидратация с молекули на разтворителя. Неполярен среди това могат да съществуват под формата на йонна двойка с противойон. В някои случаи могат да бъдат карбокатиони толкова стабилни, че са под формата на обичайните соли. Например, трифенилметил катион е сол при стандартни условия.
Решете контрол по всички предмети. 10 години опит! Цена от 100 рубли. период от 1 ден!
карбанйоните
При пускането неразделен двойка електрони при въглероден атом като междинни съединения, които се наричат карбанйоните. Те имат плоска или пирамидална структура и неразделен двойка електрони е в атомните или хибридизират орбитите. Така, наситени съединения типично пирамидални или четиристенен конфигурация, такива конфигурация тривалентен азот съединения а. Несподелени двойка електрони в метил анион заема sp3-хибриден орбити. Смята се, че за пирамидална конфигурация карбанйоните се характеризират с бързо инверсия на тетраедъра, като ефектът на "обърнати чадър" в съединенията с $ NR_3 $.
Плоският структура е типично в мястото в $ \ алфа $-позиция на анионен център $ \ пи $ -връзките, като alil- анион.
При местоположението на анионен център при въглеродния атом, директно с ненаситеност неразделен електронна двойка намира в съответните хибридизират орбитите ($ sp2- $ или $ SP- $) и не променя състоянието си на хибридизация, например в случай на винил и етинил анион-анион.
Първи карбанйоните
Един от известните методи е образуването на карбанйоните взаимодействие метал с алкилхалогениди, например:
Фигура 3. Стабилност алкилови радикали
Решете контрол по всички предмети. 10 години опит! Цена от 100 рубли. период от 1 ден!
Пишем евтини и точно навреме! Повече от 50 000 доказани професионалисти
Съобщение $ С-Li $ силно полярен (ionicity достигне приблизително 43 $ \% $) и връзката присъства под формата на йонна двойка метил анион на литиев катион и ($ CH_3 \ cdot Li + $). Ние не трябва да забравяме, че такъв запис известна степен условно, тъй като $ 57 \% $ дължи $ C-Li $ ковалентна компонент принадлежи.
Друг метод карбанйоните получени чрез взаимодействие на съединенията с silnopolyarnymy връзки ($ С-Н $ -киселина) и реагентите с основни свойства:
Фигура 4. Стабилност на алкилови радикали
Стабилността на карбанионите
Карбанионите стабилност зависи от изместването на отрицателен заряд и може да се променя, когато се поставят в $ \ алфа $ позиция на оттегляне заместителят анион център електрони с отрицателен ефект или заместители с $ \ пи $ -връзките, които показват отрицателен М-ефект. Проявлението мезомерен ефект се състои в молекулната орбитала конюгиране $ \ пи $ -връзките с прекъснат орбитален неразделен електронна двойка въглеродни атоми ($ р \ пи $ -conjugate). Ацетонил анион стабилизиране също може да бъде представен чрез резонанс структури:
Решете контрол по всички предмети. 10 години опит! Цена от 100 рубли. период от 1 ден!
Фигура 5. Стабилност на алкилови радикали
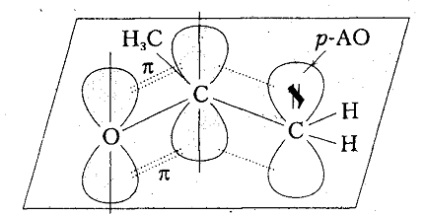
Когато се поставя в ненаситените част хетероатоми (кислород) с по-голям Електроотрицателност от въглерод, значителна част от отрицателен заряд се натрупва върху хетероатом.
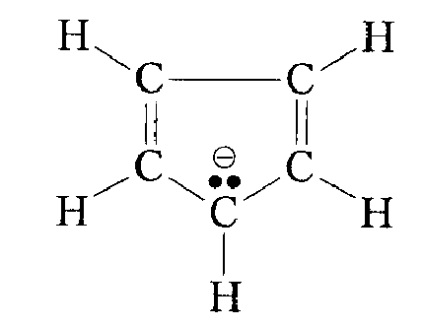
Освен това увеличава стабилността на карбанйоните повлияни ароматна система, например циклопентадиенил анион:
Фигура 6. Стабилност алкилови радикали
Освен това, карбанйоните стабилност зависи от естеството на хибридизацията на въглероден атом. Най-голям принос от $ х-AO $ в хибриден състояние, по-стабилните карбанионите, че ще се увеличи тяхната стабилност в редица SP3 $
Ефект на структурни фактори върху стабилността на аниони е обратна посока в сравнение с катиони. По-специално, стабилността на карбанионите намаляват, както следва: Първичен> вторичен> третичен.
Свързани статии
