Радиоактивността спонтанно превръщане на атома на един елемент на атоми на други елементи, придружени от емисиите на частици и трудно електромагнитно излъчване. Исторически информация. Бекерел. Изворът на 1896 френският физик A.Bekkerel направи редица доклади за откриването на нов вид радиация го (по-късно наречен радиоактивни), които се излъчват от урановите соли. Подобно на открито в продължение на няколко месеца преди рентгеновите лъчи, той имаше проникваща способност, осветява екраниран черна хартия фотографска плака и йонизиране на околния въздух. Хипотеза, която е довела до откриването на радиоактивността, Бекерел идва от под влиянието на рентгенови изследвания. Тъй като генерирането на рентгенови лъчи се наблюдава фосфоресценцията тръба стъклени стени, Becquerel Предполага се, че всеки фосфоресцентен луминисценция е придружено от излъчване на рентгенови лъчи. За да изпробвате тази хипотеза, той поставя различно фосфоресцираща субстанция на увити фотографска плака в черна хартия и получи неочакван резултат: осветената беше единствената плоча, която е в контакт с кристал на уран сол. Многобройни експерименти за контрол показват, че причината за излагане не е фосфоресцираща, а именно уран, той може да бъде в каквито и химически съединения. радиация свойство да предизвика йонизация на оставя заедно с фотографски метод за запис по-удобен метод за електрически, което значително ускорява процеса на изследване въздуха.
Кюри. Използване на електрически метод, G. Schmidt и М. Кюри в 1898 торий радиоактивност намерено елемент. На следващата година Дьобиерн открил елемент актиний радиоактивни. Стартира съпрузи P. и M.Kyuri системно търсене на нови радиоактивни вещества и да се изследват свойствата на емисиите им потвърждават Becquerel предполагам, че радиоактивността на уранови съединения е пропорционална на броя съдържа в уранови атоми. Между изследваните минерали, този модел се нарушава само от рудата смола уран (uraninite), което е четири пъти по-активен от съответното количество чист уран. Кюри заключи, че uraninite трябва да съдържа силно неизвестен елемент. След щателно uraninite химично разделяне на компоненти, те открили, радий, химични свойства, подобни на барий, и полоний, който е известен с бисмут.
Ръдърфорд. В по-нататъшни проучвания на радиоактивност водеща роля принадлежи на Ръдърфорд. Фокусирайки се върху изучаването на това явление, той установи естеството на радиоактивни трансформации и придружаващите радиация.
Емисията на радиоактивни вещества. Физически радиоактивни елементи отделят три вида радиация: алфа, бета и гама. През 1899, Rutherford идентифицирани алфа и бета радиация; година по-късно отвори P.Viyar гама-лъчение.
Алфа радиация. Въздухът при атмосферно налягане, алфа радиация преодолява само на малко разстояние, обикновено между 2,5 и 7,5 см. В вакуум електрически и магнитни полета забележимо отклоняват от първоначалната си траектория. Посоката и степента на отклонения показват, че алфа радиация - поток от положително заредени частици, за които заряда към маса (д / т) точно съответства на два пъти атом йонизиран хелий (He ++). Тези данни и резултатите от проучвания спектроскопски събрани алфа частици право Rutherford да се заключи, че те са ядрата на хелиеви атоми.
Бета радиация. Това облъчване е по-голяма проникваща способност от алфа радиация. Както алфа радиация, тя се отклонява в магнитни и електрически полета, но в обратна посока и по-голямо разстояние. Това показва, че бета-лъчение е поток на отрицателно заредени ниска маса частици. Във връзка д / m Rutherford идентифицирани бета частици като обикновени електрони.
Гама радиация. Гама радиация прониква в материала по-дълбоко от алфа и бета радиация. Не се отби в магнитно поле, и затова няма електрически заряд. Гама лъчите са идентифицирани като твърд (т.е., с много висока енергия) на електромагнитно излъчване. Разделяне на радиоактивни лъчения в магнитното поле на алфа-, бета- и гама-лъчи са показани схематично.
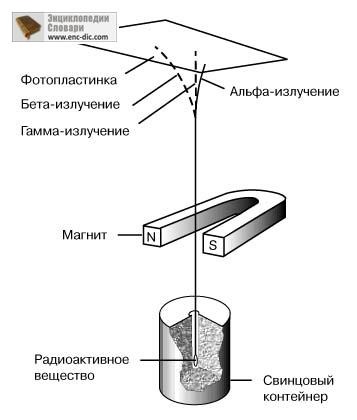
СХЕМА експерименти илюстрират отклонението на различни видове радиация в магнитно поле.
Теорията на радиоактивното разпадане. По време на излъчване на емисиите вещество претърпява няколко промени. Например, емисиите радий придружава от освобождаването на радон газ ( "излъчване"). На свой ред, радон разлагащата се оставя радиоактивни отлагания по стените на съда, съдържащ. Събрани от разпада на радий еманация губи половината от първоначалната дейност в около 4 дни. Тези и други не се поддават на тълкуването на опитните факти може да се обясни с теорията на радиоактивното разпадане на атома, предложени от Rutherford и Соди през 1903 г., както и за преместване на правилата, формулирани в 1913 A.Rasselom и независимо от фаянс и Соди. Същността на Ръдърфорд и Соди теория е, че превръщането на един химичен елемент, в резултат на радиоактивния разпад в друга.
компенсира правило. компенсира правило определя точно какъв вид трансформация претърпява химичен елемент, излъчваща радиоактивност.
Емисията на алфа и бета частици. компенсира правило може да се обясни с помощта на ядрения модел на атома, предложен от Ръдърфорд през 1911 г. Според този модел, в центъра на атома е положително зареден ядро, което съдържа по-голямата част от масата на атома. Електроните се въртят около ядрото, таксата, която компенсира положителния заряд на ядрото. Всеки атом се дължи на неговата атомен номер Z, съответстващи на номера на последователност на периодичната таблица и числено равно на ядрен заряд, изразена в единици за електронен заряд. Един алфа частиците е Z = 2 и масовото число (закръглено атомно тегло) А = 4. Ако нестабилна ядро излъчва бета частиците му Z се увеличава и масовото число, не се променя. Следователно, радиоактивният атом, се превръща в следващата атом на периодичната таблица, за. Когато емисия на алфа частици и Z А новообразуваната ядро намаляване на 2 и 4 единици, съответно, и на детето атом опит подходящ изотопно преобразуване "измества" наляво в Периодичната таблица на елемента майка.
Гама радиация. Орбиталните електрони, които получават повече енергия, за да могат да се движат по-високи нива на енергия. Връщайки се към основния (нормално) състояние, те дават излишната енергия като светлина или рентгенови лъчи. Ядрата на атоми, които имат излишък енергия може да се прехвърлят във възбудено състояние. Такова възбуждане често опит ядро, образувана по време радиоактивни превръщания. Обръщайки се към основното състояние, те излъчват излишната енергия под формата на гама лъчи. От особен интерес е вариант на колапса, когато радиоактивно ядро има дълъг живот на възбудено състояние. В този случай, същите ядра (с едни и същи стойности на Z и А), са в Наблюдават радиоактивни разпадания от същия тип, различни енергийни състояния, но те се срещат с различна скорост, тъй като някои от развълнувани ядра гниене, а други от основното състояние. Това явление се нарича ядрено изомерия, и възбудени и нормални ядра се наричат изомери.
Decay верига. изместване обикновено възможно да се проследи превръщането на естествените радиоактивни елементи и изграждане на три от тях родословно дърво, предците на които са уран-238, уран-235 и торий-232. Всяко семейство започва с много дълъг живот радиоактивен елемент. Уранът семейство, например, уранови глави с масовото число 238 и период на полуразпад от 4.5 * 10 9 години (Таблица. 1 в съответствие с оригиналното име е определен като уран I).
Таблица 1.
Радиоактивни семейства УРАН
Периодът на полуразпад. Най-важната характеристика на радиоактивен атом е живота й. Според закона на радиоактивното разпадане, вероятността, че за определен период от време ще разпадането на един атом, е постоянна. Следователно, броят на разпада срещащи всеки втори пропорционално на броя на атоми, и закона, който описва процеса на разпадане, е експоненциално. Ако времето Т пада половината от първоначалния размер на радиоактивни атоми, останалата половина от атомите разпадат по време на следващия интервал от време на същия период. Време T е времето на полуразпад на радиоактивния елемент. За различни елементи е полу-живота на десетки милиарди години, за да милионни части от секундата или по-малко.
Уранът семейство. На елементите на семейството на уран може да се проследи повечето от разгледаните по-горе на радиоактивни трансформации свойства. Например, третият член на семейството има ядрена изомер. Уран Х2, излъчващ бета частици се превръща уран II (Т = 1,14 мин). Това съответства на бета разпад на възбудено състояние на протактиний-234. Въпреки това, в 0,12% от случаите възбудени протактиний-234 (уран Х2) излъчва гама квантовата и преход към основното състояние (уран Z). Бета-разпад на уран Z, също води до образуване на уран II, се среща в 6.7 часа радий C интересни, които могат да се разпадат по два начина. Излъчващ, или алфа или бета частици. Тези процеси се конкурират помежду си, но 99,96% на бета разпадане настъпва за образуване на радий С ". В 0,04% С радий излъчва алфа частица, и се превръща в радий C" (РКС "). От своя страна рацемичен "и Rac" от емисиите на алфа и бета частици, съответно, се преобразуват в D. радий изотопи. Сред членовете на семейството на уран са такива, чиито атоми имат един и същ атомен номер (същия заряд ядра) и различни масови числа. Те са идентични в техните химични свойства, но се различават по природата на радиоактивност. Например, радий В, D и радий, радий G, имащ същия атомен номер с олово 82, като олово в химическата поведение. Очевидно е, че химичните свойства не зависят от броя на маса; те се определят от структурата на електронен слой атоми (и следователно Z). От друга страна, масовото число, е от решаващо значение за стабилността на ядрената радиоактивни свойства атом. Атомите с еднакво атомно число и различни масови числа, се наричат изотопи. Радиоактивни изотопи на елементите са били отваряни, Соди през 1913 г., но скоро F.Aston от мас-спектроскопия, показа, че изотопите са стабилни и имат много елементи.
Други естествени радиоактивни елементи. Всички елементи от периодичната таблица на бисмут (т.е., с Z> 83), са радиоактивни. Подобно на уран-238, уран-235 с дълъг живот и торий-232 и актиний, съответно се запътили семейство радиоактивен торий. При естествени условия има уран, торий и техните дъщерни радиоактивни продукти. Това се дължи на факта, че периодите на полуразпад на предците на семейства са сравними с възрастта на Земята, и те не са напълно се срина. Химични елементи с атомни номера> 92 са получени в лабораторията в резултат на ядрени реакции и е установено между термоядрени продукти експлозия, и всички те са радиоактивни. Сред по-леки елементи има няколко естествена радиоактивност. Полуживотите те са толкова големи, че те все още съществуват на Земята в значителни количества. Радиоактивно калиев-40 чрез излъчващ бета частица се превръща в стабилна калций-40 (Т RADIOAKTIVNOST10 9 години). Въпреки това, той може да се разпадне чрез електронно улавяне и се превръща в аргон-40. Бета активност рубидий-87, пробивайки (Т RADIOAKTIVNOST6 х 10 10 години), преминава в стабилен стронций-87. Естествено срещащи самарий-152 - само лек от бисмут, радиоактивен елемент, който излъчва алфа частици. Неговият период на полуразпад период - от 10 до 12 години. В елементи с атомни номера 43, 61, 85 и 87, без стабилни изотопи, без дълголетни предшественици, така че те не се намират на Земята. В много дълготраен изотоп на технеций (Z = 43), времето на полуразпад - около 300 000 години, което е значително по-малка от очакваната възраст на Вселената. Въпреки това, значителна част от технеций е намерено в състава на звезди спектрален тип С. Този факт се тълкуват като ясно доказателство на факта, че те се проведе сравнително наскоро активни еволюционни процеси.
Изкуствен радиоактивност. Алфа-частици бомбардират атоми на азот, и J. Е. Rutherford. Chadwick през 1919 г. за първи път реализира ядрената реакция, което води до превръщане на азот към кислород. С появата на ускорители на частици предните проучвания за ядрени реакции разширяват значително. През 1934 г. Фредерик и Ирен Жолио-Кюри открива изкуствената радиоактивност и режим на позитронна разпад. Те откриват, че алфа-облъчени частици от борен, магнезий и алуминий са превърнати до радиоактивни изотопи на други елементи, гниене се придружава от емисиите на позитрони (д +). Например, когато бомбардирани с частици алфа двуалуминиев триоксид произведени радиоактивен фосфор-30, която се разпада (Т = 2,5 мин) излъчва д + и се превръща в стабилна Si-30. Позитрон открит през 1932 K.Andersonom космическите лъчи, генерирани в средното радиация е частица от теглото и размера на електронен заряд идентични, но с положителен електрически заряд (електрон античастици). Когато позитрон излъчващ радиоактивен атом ядро на серийния номер на атом се намалява с една и масовото число, остава непроменена.
улавяне Electron. Capture ядро на една от орбиталните електрони еквивалент емисията на позитрон: маса брой атом не се променя, и заряд на ядрото намалява по един. Електроните К и Л черупки са толкова близо до мозъка на костите, в някои случаи, улавяне на електрони, като механизъм за радиоактивното разпадане, започва да се конкурира с емисиите на позитрон. Що се отнася до залавянето на електрон отнема по-малко енергия в сравнение с еквивалентен позитрон разпад, понякога, като в случай на берилий-7 (вж. Таблица. 2), то е възможно енергично заснемане само на електрони.
Таблица 2.
Някои свойства светлина атома
Информация за светлинните стабилни и радиоактивни атоми са представени в таблица. 2, където Z - атомен номер, А - масово число. Информацията в таблицата се изразява в атомни масови единици въглерод. Скалата за енергия е равна на 931.162 MeV. Атомна маса характеризира стабилност атом. Ако двете атоми имат една и съща маса брой и различни атомни номера (isobars), по-тежки от isobars ще бъдат нестабилни по отношение на гниене в запалка. Например, тритий-3 се превръща в хелий-3, въглерод-11 - в бор-11.
Използването на радиоактивност.
Medicine. Радий и други природни радиоизотопи са широко използвани за диагностика и радиотерапия на рак. Използването за тази цел изкуствени радиоизотопи значително повишава ефективността на лечението. Така например, радиоактивен йод се въвежда в организма като разтвор на натриев йодид, които селективно се натрупва в щитовидната жлеза и поради това се използва в клиничната практика за определяне на функцията на щитовидната жлеза и нарушения в лечението на болестта на Грейвс. Използване на белязано измерва скоростта на кръвния поток е решена и пропускливост на кръвоносните съдове на крайниците натриев физиологичен разтвор на. Радиоактивно фосфор се използва за измерване на кръвния обем и лечение eritremii.
Research. Радиоактивни етикети, в много малки количества, въведени в физични или химични системи ви позволяват да се следи всички промени, настъпили в тях. Например, за израстване на растение в атмосферата на радиоактивни въглероден диоксид, химици могат да разберат фините детайли на образуването на сложни въглехидрати в растенията от въглероден диоксид и вода. В резултат на непрекъснато бомбардиране на земната атмосфера от космическите лъчи с висока енергия азот-14 е в своята улавяне на неутрони и протони, излъчващи превърнати в радиоактивен въглерод-14. Ако приемем, че интензитетът на бомбардиране и следователно равновесното количество въглерод-14 в последния Милениум остава постоянно и дава С-14 полуживот период от остатъчният активност, може да се определи възрастта на намерени животински и растителни остатъци (метод радиовъглеродно). Този метод е бил успешен с високо доверие към днешна дата намери паркинг праисторическия човек, имаше преди повече от 25,000 години.
Вижте. Също така
Структурата на атома;
Пиер Кюри;
Радиовъглеродно датиране.
СПРАВКА
Доктрината на радиоактивност. История и съвременност. М. 1973 ядрена радиация в областта на науката и технологиите. 1984 М. Furman VI Alpha гниене и свързаните с ядрени реакции. М. 1985
Помощ за Търсене на двигатели
Свързани статии
