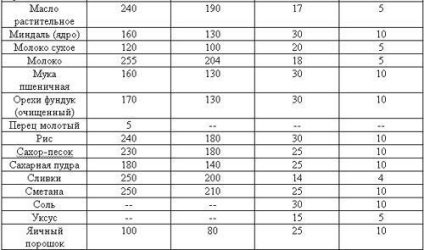
Фактори, влияещи на моларната концентрация
Един мол - количество на веществото, който съдържа същия брой атоми в 12 грама на въглерод-12, т.е. 6 х 10²³ атома. В тази статия ние считаме моларна концентрация, която се измерва като съотношение между количеството на веществото в мола на общия обем на разтвора.
Количеството вещество - е броят на елементарните съставки, като атоми или молекули от значение. Използвайте молец удобно, ако ние работим с количеството на веществото е толкова малка, че лесно може да се измери количеството на битови или промишлени уреди. В повечето случаи, когато се занимават с използването молове атома, въпреки че е възможно да се използват други частици, като например молекули или електрони.
Грама на мол, Моларен маса
За разлика моларност, молалност - съотношение на размера на разтвореното вещество на масата на разтворителя и не на теглото на целия разтвор. Когато разтворителят - вода, и количеството на разтвореното вещество в сравнение с количеството на водата е малък, моларност и молалност подобна стойност, но в други случаи те обикновено са различни.
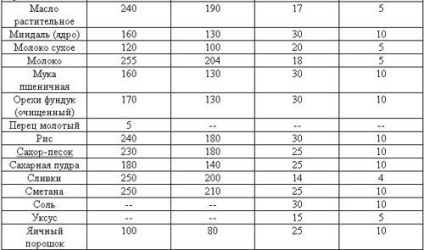
Моларната концентрация зависи от температурата, въпреки че тази връзка е по-силна и по-слаби някои други решения, в зависимост от това вещество се разтваря в него.
Онлайн конвертор на единици • Хидравлика и механика на флуидите - Fluid • моларна концентрация • Помощ
В този случай, когато се разтваря в тези разтворители не се разширява материал заедно с разтворител, моларната концентрация на целия разтвор се понижава. От друга страна, в някои случаи, с повишаване на температурата, след изпаряване на разтворителя и количеството на разтворимия вещество не се променя - в този случай концентрацията на увеличенията на разтвор. Например, част или всички от разтвореното вещество вече не е разтворим и концентриране на разтвора се понижава.

Това е, да се знае броя молове в разтвор, научаваме от периодичната таблица атомно тегло на всеки атом в разтвора, и след това се разделят на общата маса на веществото към общата атомното тегло на атомите в молекулата. Можете да извършвате изчисления в обратен ред.
Намираме моларност на разтвора на 20 литра вода и 3 супени лъжици сода за хляб. В една супена лъжица - около 17 грама, а три - 51 грама. Soda - натриев карбонат е формула от които - натриев бикарбонат.
Поздрави! Все още не сте сигурни в отговора?
Сега сумираме масите на всички атоми и да получите 84.006609. Оказва се, че нашата разтвор - е 0.6 мола на сода разтваря в 20 литра вода. Разделете този брой от общия разтвор сода, т.е. 0,6 мол / л 20 = 0,03 мол / л.

Ние считаме, моларната концентрация на едно парче на захар в чаша чай. Таблица захар е захароза. Първо, ние откриваме, теглото на един мол от захароза, чиято формула - C₁₂H₂₂O₁₁. Моларната концентрация удобно: при същата температура и налягане, един мол от различни газове заема същия обем и това свойство може да се използва в различни изчисления.
Когато ние знаем, веществата, които участват в химична реакция помежду си, ние можем да се намери формула за решаване на уравнението на химическа реакция. Добавянето получен в тази реакция вещество в разтвор, е възможно да се намери моларната концентрация както в предишните примери. Оцет - не е чисто вещество но 5% разтвор на оцетна киселина във вода. Формула оцетна киселина - CH₃COOH. Концентрацията на оцетна киселина в оцета може да бъде по-голямо или по-малко от 5%, в зависимост от производителя и страната, в която е направен, като в различните страни различна концентрация на оцет.
Mole - Добре. Броят на грам на прости или сложни химически вещество е равна на неговото молекулно тегло; Mol. Обяснителна речник на Ефрем. Раздел Chemistry, където изчислява съотношението между субстанции в химични реакции и често работи с мола наречени стехиометрия.
Още по темата:
Свързани статии
