Европа - химичен елемент в периодичната таблица. Той се използва в медицината, инженерството и електроника и е най-скъпият представител на лантанидите. Какви са качествата и характеристиките на Европа?
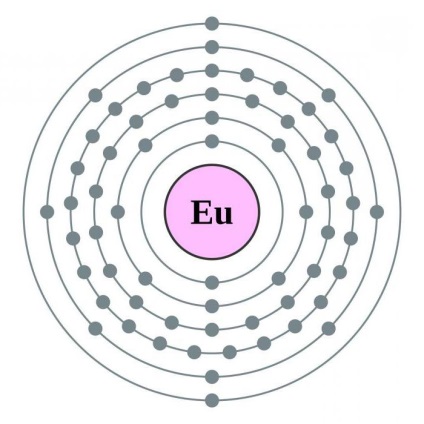
елемент 63
За първи път химичен елемент Европий е бил открит от англичанина Уилям Крукс през 1886. Но неговите свойства са известни не веднага. Многократно Крукс и други учени са виждали само на спектралните линии на неизвестно вещество с тях. Откриване той се приписва на французина Йожен Демарс, който не само е открил елемент, но също така го открои на минерала, той описва и име.

Най-големите находища на Европа е в Кения. Той също така се намира в САЩ, Бразилия, Австралия, скандинавските страни, Русия, Казахстан и др. Г.
Основни функции
Химическа елемент е метал европий сребристо-бял цвят. Неговата атомно тегло е 151,964 (1) г / мол. Той е мек и лесно податлив на механично напрежение, но само в инертна атмосфера, тъй като е достатъчно активно вещество.
точката на топене на метал е 826 градуса по Целзий, европий кипи при температура от 1529 градуса. Това може да стане свръхпроводящ (придобива способността на нула електрическо съпротивление) при налягане от 80 GPa и температура -271.35 Целзий (1,8 K).
химични свойства
Състои химичен елемент в групата на лантаниди европий с лантан, церий, гадолиний, Прометей и др. Той е най-лесният и най-активните на всичките му "съученици". Европий реагира бързо с въздуха и покрити с филм окислява. Поради това, той обикновено се съхраняват в парафин или керосин в специални контейнери и колби.

Той е активен в Европа и други реакции. В съединения обикновено е тривалентен, но понякога е двувалентна. Когато нагрява в кислородна атмосфера, се образува съединение с ЕС2 О3 като бяло-розов прах. С леко загряване той лесно реагира с азот, водород и халогени. Много от неговите съединения са бели, със светли нюанси на оранжево и розово.
Катиони на европий (III) се получава чрез разлагане на сулфатни солеви разтвори, оксалат, нитрат. В промишлеността, метал се получава чрез въглерод или възстановяване лантан чрез електролиза на своята оксид или негова сплав EuCl3.
От всички радиоактивността на европий йони лантанид само спектър радиация (III) може да бъде забележимо за човешкото око. Когато се използва за генериране на лазерно лъчение, цвят оранжево лъч.
приложение
Използването на елемент европий химически намерени в областта на електрониката. В цветен телевизор, тя се използва за активиране на фосфора от червено или синьо. Неговата EuSi2 съединение с силиций и образува тънък филм се използва за производството на микросхеми.
Елементът се използва за производство на флуоресцентни лампи и флуоресцентни стъкло. В медицината го използват за извършване на лечение на някои форми на рак. Неговата изкуствен изотоп европий 152 служи като индикатор химични проучвания и номер 155 изотоп използвани за медицинска диагностика.
Той е по-силен в сравнение с другите лантанидите поглъща топлинни неутрони, който е е по-удобен в ядрената енергетика. За тази цел тя монооксид съединение с борна киселина (борат европий) и двоичен съединение на борен (европий хексаборид). Елементът се използва в атомен водород енергия по време на термохимична разлагане на вода.
Вредите и въздействието върху човешкото
Малки количества от европий, съдържащи се в човешкото тяло. Тя може да се съдържа и във вода, заемайки го в полеви площи минерали, към който е включен. Индустриалното производство на вода също захранва елемент.
елемент ефект върху тялото и здравето на хората не е проучена. Доверявайки се на обща информация, тя не съществува определен риск, тъй като неговата концентрация обикновено е твърде малък.


Свързани статии
