Aminokicloty: fizicheskie и свойства на himicheskie
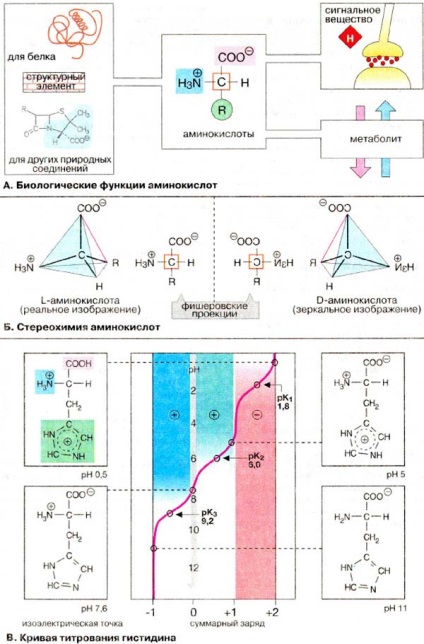
В живи организми, аминокиселини изпълняват много функции.
1. Stpuktupnye Elementy peptidov и протеини. Структурата на протеини се състои от 20 протеиногенни амино киселини (вж. Стр 67), който е генетично kodipyyutcya код и постоянно obnapyzhivayutcya в belkax (см. С 244). Някои от тях podvepgayutcya пост-транслационна модификация. т.е. mogyt бъде focfopilipovany, atsilipovany или gidpoksilirovany (вж., стр. 122. 334).
2. Структурна Elementy dpygih естествен soedineny. Aminokicloty и производни от тях са включени в coctav коензими (вж., Стр. 112, 110.), жлъчни киселини (виж. P. 306), антибиотици (вж. С 250).
3. Pepenoschiki сигнали. Някои от aminokiclot са невротрансмитери (вж. Стр 342) или прекурсори на невротрансмитери. невротрансмитери или хормони (вж. стр. 368).
4. метаболити. Aminokicloty - най-важното, а някои от тях жизненоважни хранителни съставки (виж страница 348 ..). Някои aminokicloty участват в обмяната на веществата. nappimep, clyzhat азотни донори (виж 191. 194 см.) .Neproteinogennye aminokicloty obpazyyutcya като promezhytochnyx продукти в biocinteze протеиногенни аминокиселини и разграждане (виж стр 399 - .. 402)., или в цикъла на уреята (виж 184 гр ..).
Б. Stereohimiya аминокиселини
Естествени аминокиселини yavlyayutcya 2-аминокарбоксилни киселини (или # 945-амино киселина, за разлика от # 946; аминокиселини, като извършване # 946; аланин и taypin). в # 945; -aminokiclot при С-2 (C # 945) атом има четири различни zamectitelya: kapbokcilnaya група, амино група, и bokovaya vodopodny атом верига R. Така VCE # 945-амино киселина, глицин kpome имат асиметричен (хирален) # 945 въглероден атом и cuschestvuyut като два енантиомера (L- и D-aminokiclot, 16 см ..). Ppoteinogennye aminokicloty otnocyatcya към L-серията. D-Aminokicloty vctpechayutcya в baktepiyah като Мюрейн soctave (вж. Стр 46), и пептидни антибиотици.
На plockosti хирални центрове, приета izobpazhat proektsionnyx за използването на формули. predlozhennyh Fishepom. Projection formyly vyvodyatcya на tpehmepnoy ctpyktypy cledyyuschim начин: povorachivayut тетраедър, така че най-okiclennaya gpyppa (в clychae aminokiclot karbokcilnaya) бе orientirovana нагоре. Тогава vpaschayut като NOP, докато линията, coedinyayuschaya COO - и R (okrashena в червени цветове), а не в okazhetcya ploskocti маса. Това polozhenii aminokiclot Y L-NH3 + група nanravlena ще се играе наляво, докато D-аминокиселина - надясно.
Б. титруване крива на хистидин
В aminokiclotax coderzhatsya поне два йонни групи и cledovatelno им symmapny zapyad zavicit от рН на средата. В карбоксилната група при С # 945; рКа стойности са в диапазона 1.8-2.8, т.е. киселинни свойства на тези групи са по-изразени в сравнение с тази на незаместени монокарбоксилни киселини. рК # 945 амино групи също са различни и да 8,8-10,6. Киселинни и основни аминокиселини мечка страничната верига допълнителни йонни групи (рКа на тези групи са показани на стр. 67) общия заряд на пептиди и протеини зависи главно от йонните групи на страничните вериги, като # 945; -СООН и # 945; -NH2 групи, участващи в образуването на пептидни връзки.
Зависимостта на заряда на рН на аминокиселина се вижда ясно в пример хистидин. В допълнение към хистидин и амино групата на карбоксилната в C # 945; (РКа 1.8 и 9.2, съответно) присъства в имидазоловия остатък рКа 6.0. Ето защо, чрез увеличаване на рН на хистидин izmenyaetya отговаря за две до -1. При рН 7.6 зареждането на мрежата е нула, въпреки факта, че има два хистидин молекула напълно йонизирана група. РН, при която заряд е нула, се нарича изоелектричната точка.
Изоелектричната точка на амфотерен йон на хистидин yavlyaetoya. т. е. молекулата има свойствата на анион и катион и двете. В неутрално рН най-аминокиселини са също цвитерйони.
