Законът на равномерно разпределение на енергията върху степените на свобода: енергията на мол-ку-Ly равномерно разпределени STE-пе-Yum свободата на, т.е. всеки свобода STE-пън, независимо от структурата на Con-ционни молекули имат същата енергия, ravnayakT / 2.
Клаузиус
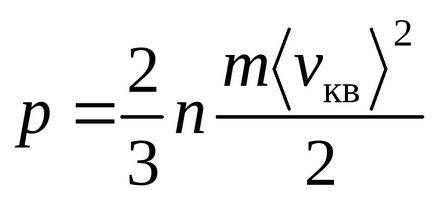
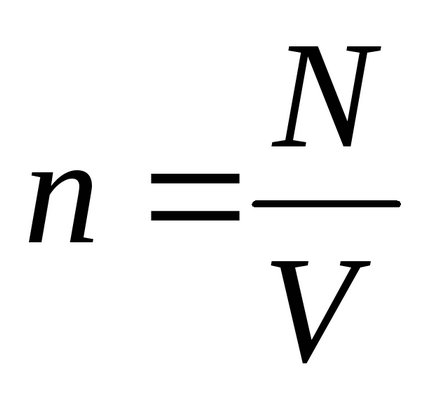

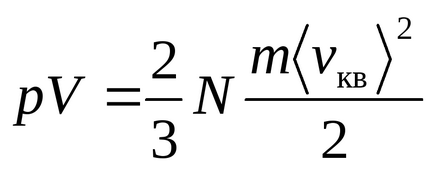
Уравнение Менделеев - Клапейрон
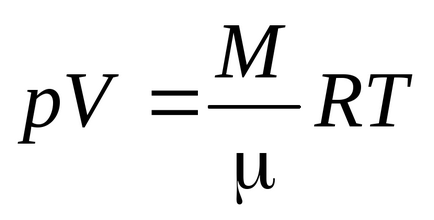

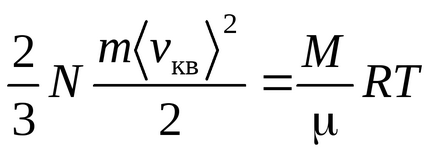

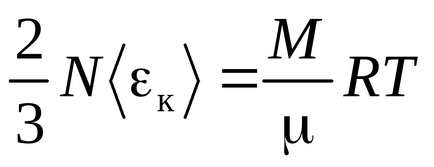

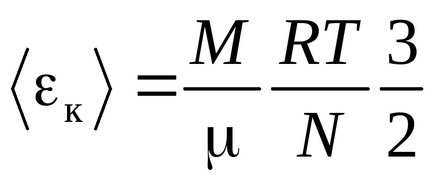
Clausius уравнение се получава на предположението, че газовите молекули - материални точки (моноатомни молекули) с три степени на свобода на транслационно движение. Тъй като всички пътни направления на са еднакво вероятни, общата енергия на молекулата се разпределя по равно между трите степени на свобода и за всяка степен на свобода КТ / 2 енергия
Енергията на една молекула:
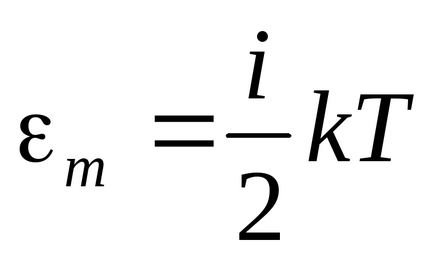
Енергията на един kilomole :.
Енергията на произволна маса на газ
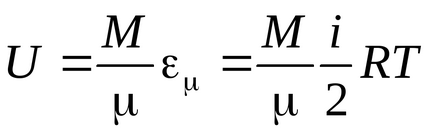
3. Работната и топлина. Топлина, неговите видове.
Елементарно работа. направено от газа, когато буталото е преместен DH на сегмента,
Проучванията при крайния изменението на обема газ от V1 към V2,
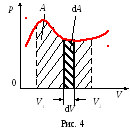
Ако DV> 0, DA> 0: Системата работи на външни органи - дава им някои от тяхната енергия.
Ако DV <0, то dA <0: внешние тела совершают над системой работу – система получает энергию извне.
Графично, операцията е показано на р и V координати (структура на потока) на областта, ограничена от крива р = F (V) и две ординати съответстващи чал-но-ти V1 и краен обем V2.
Прехвърлянето на топлинна енергия (топлина) се придружава от промени в температурата на тялото. Характеризира се с по-по-цифра-тикове органи способност за привличане на неговата температура, вследствие на топлината, получена от външната страна се въвежда понятието за специфична топлина.
TeploemkostS- скаларна физическа величина, връзката Характеристики-rizuyu-schaya между количеството топлина предава към системата и промяната на температурата.
видове топлинна мощност
Пълен teploemkostSpol числено равна на количеството топлина, което трябва да бъде прехвърлен в системата, за да се повиши температурата с един градус
Моларен teploemkostS числено равно на количеството топлина, което трябва да бъде съобщено един Kmol на вещество за повишаване на температурата от една степен:
Специфичен топлинен капацитет (С) е числено равно на количеството топлина, които трябва да бъдат докладвани на единица маса на веществото за повишаване на температурата от една степен:
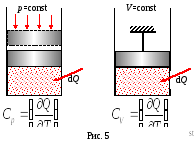
В зависимост от природата на процеса се отличават топлина при постоянен обем CV и при постоянна davleniiSr.
Физическа работа на разширяване е smyslR- 1 мол идеален газ в изобарен процес чрез загряване до 1 ДА
