преработката на нефт и газ технология. част 1
Реакционната парафинови въглеводородни изомеризация са равновесие-ТА:
Те се появяват с малка или никаква промяна в обема, така термодинамиката-динамично равновесие зависи само от температурата; температура бла образуване ниско gopriyatstvuyut изопарафинови въглеводороди. Топлинният ефект на изомеризация реакцията е малък - от 2 до 20 кДж / мол - и променя малко с температура neniem-измерими. Проучването на равновесие изомеризация пара-въглеводородни финландци посветен значителен брой експериментални творби-ТА и дизайн характер. Наблюдавано за някои въглеводороди несъвпадение се дължи на недостатъчно точно изчисляване на термодинамична количества-Ing. При изчисляването на равновесни състави от стойностите на равновесните константи равна-он трябва да се счита, че на практика, по време на протичането на изомеризация реакцията не винаги е оформен всички теоретично възможни изомери от тях; за-пример, само два изо-мерни продукти бяха открити в изомеризацията Pontano - п-пентан и изопентан (2-метилбутан); неопентан (2,2-диметилпропан) не се открива. Последното се дължи на нестабилността на първичен carbocation на - изисква стъпка прегрупиране вторичен carbocation. С оглед на пеопентан баланс отсъствие-Следствие трябва да се разглежда само между н-пентан и изо-пентан. Същото важи и за изомерите на хептан: про-серия изомеризация не 2,2-dimethylpentane, 3,3-dimethylpentane, W-етил-пентан, поради естеството на кинетичната трудности.
константи на равновесието на реакции на изомеризация С4-С6 парафини, ental Пия изомеризация и изомеризация изменение в ентропията, изчислени на данните за Ba-Ваня спектроскопски и на свободните енергии на данните, показани в таблица. 5.8 и равновесието състави на смеси от изомери - в таблицата. 5.9. При изчисляването на равновесните константи на изомеризация реакцията използване на разликата в свободните енергии на изомери:
J / (мол К), и равновесната константа Кр за реакцията на изомеризация на парафинови въглеводороди с С4-С6 в газовата фаза
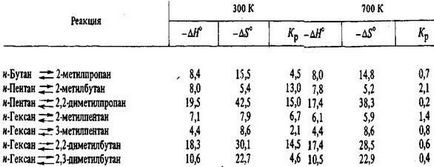
Съставът на равновесната смес се изчислява въз основа на константите на равновесие на всеки въглеводород изомеризация в друга:
Таблица 5.9 Mass състав (%) на равновесната смес от изомери С4 -С6 парафини
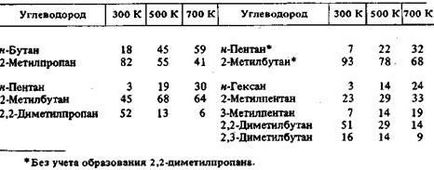
Кинетика и механизъм на изомеризация реакцията зависи от вида на катализатора и условията на реакцията. В контекста на хетерогенна реакция катализа на постъпления парафин изомеризация от термодинамично контролиран механизъм. Количествена оценка на кинетичните параметри на реакцията на въглеводороди, е способността на въглехидрати преобразуване на постоянна скорост в едър въглеводород изомер или изомерна смес. Изследване на начини и състав на тези преобразувания междинни съединения, свързани с реакцията на проучване фур-nism.
При осъществяване на изомеризация на парафинови въглеводороди с про-мислене aljumoplatinovyh катализатори насърчавани с флуор и хлор metalltceolitnyh катализатори и superacids, особено кинетиката на реакцията и механизъм на механизма за образуване причинени от PROM-diate съединения.
Няколко механизми образуване carbocation, един от тях се намалява до междумолекулно трансфер хидрид:
Има друга гледна точка, съгласно която карбокатиони, могат да бъдат образувани чрез разцепване на парафини хидрид Lewis Ки слотове:
В този случай, изображения могат vatsya газ рекомбинация водород чрез протонен и хидрид йон.
Изомеризация на парафини в sverhkisdotnyh среда става чрез протонирането на парафинов въглеводород -връзките S, при което се образува некласически карбониев йон с две-електронна връзка trehtsen-ването, последващо отцепване на което води до по конвенционален три координиран carbocation и водород:
Механизмът на изомеризация на бифункционални катализатори. механизъм Rassmat-rivaya реакция на изомеризация на парафини би-функционални катализатори soderzhadih Група VIII метали могат да поемат три типичните случаи, в зависимост от киселинността на средата:
на катализатори с много силна киселинност носители изомеризира-ЛИЗАЦИЯ появява на местата на киселина, ролята на метала се редуцира до ограничение-cheniyu образуването на кокс и профилактика на деактивиране на киселина обекти; Пример за това е процес aljumoplatinovyh валцувани-сладко повишен с хлор;
на катализатори с много ниска киселинност изомеризация среда се среща само в металните центрове и механизма на реакцията зависи от метал ситото на кристалита размер;
на катализатори леко-киселинен носител като плащане на аморфен силициев двуокис-двуалуминиев триокис или флуориран алуминиев изомеризация се осъществява чрез обичайните механизъм -education бифункционални междинни съединения в метални части II zomerizatsiya-олефини на киселина сайтове.
Ако изомеризация се извършва на металната повърхност, механизмът се различава от Otley-би-функционална. В случай на бифункционален механизъм в AD-парафинов въглеводород сорбция върху металната повърхност включва два съседни въглеродни атоми на парафинов въглеводород може да се разцепват два атома водород до образуване на олефин в газова фаза, олефин адсорбираното може да бъде подложен на хидрогенолиза. Ако са възможни парафин адсорбирания въглеродни атома, Мами, които не са в съседство, но образуването на вой-С-С-връзка, в резултат на пет- или шест-членни циклични въглеводороди, и тяхното последващо отваряне чрез счупване на друг С-С връзка. За такава реакция е необходимо въглеродните атоми, свързани с повърхността се разделят с четири или пет въглеродни атома и са свързани към два съседни метални атоми. Възможността за такава реакция е открита от Гуо и Андерсен. Реакционната последователност в тази фур-nism изомеризация следва:
две несъседни С-Н връзки се разграждат и въглеводород се адсорбира върху повърхността на въглеродните атоми, свързани към съседни центрове IU талий;
Обратна връзка С-С, образуван между два въглеродни атома адсорбирания прът, което води до образуването на циклопентан или циклохексан-нула пръстен, който може да се десорбира;
циклични частици могат отново адсорбирани върху повърхността или месят въглеродни атома, които са свързани с повърхността на Дрю-Gie без десорбция, и С-С връзка може да се разкъса;
4) добавяне на водороден атом и десорбция на частиците на адсорбираните без образуването на С-С връзки води до скелетна изомеризация на п-хексан, 2-метилпентан.
Фиг. 5.16 показва схема за изомеризация на парафини С6 върху металната повърхност.
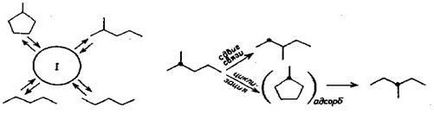
Схема Ris.5.16 хексан изомеризация реакции на металната повърхност: I - пет-
titichlennoe пръстен на повърхността.
Фиг. 5.17 Комуникация и цикличен смяна изомеризация на 2-metillentana - 2-13C. вие любезен мисли за комбиниране двуфункционално киселина и мет-nisms да platinomordenitsoderzhaschem катализатор.
Вторият механизъм за изомеризация на парафини метали се дължи механизъм смяна. Това осигурява образуването на а-, а-, г -triadsorbirovannyh съединения, свързани с два съседни метални атоми. Изомеризация на не-opentana трябва да включва адсорбция върху две метални атоми образуване на връзка между въглеродните атоми на повърхността и пробие една от връзките в съ - живее пръстен циклопропан да се образува 2-метилбутан.
Проучване изомеризация реакция се използва радиоактивен изотоп възможно хексани 13С да се определи съотношението на механизмите на реакцията и комуникация циклична промяна в зависимост от изомеризация катализаторни свойства. Квалификация платина размер кристалита на катализатора показа, че в случай на кристалити по-малки от 2 пМ преобладават цикличен изомеризация и хидрогенолиза neselek-тивна метилциклопентан, докато в по-големи кристали доминира срязване връзки и селективен хидрогенолиза.
Относителното съдържание на метал и киселина сайтове определя дали реакционната Michiru стадий.
