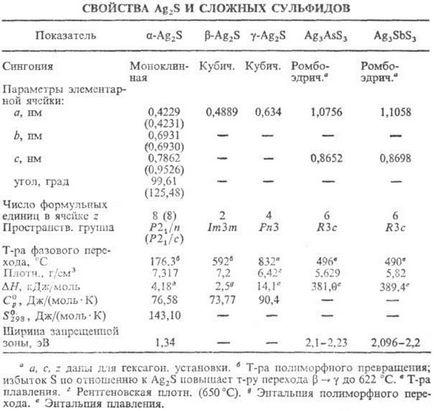
СРЕБЪРЕН сулфид AG2 S, на сиво-черен кристали; съществува в три модификации (виж таблица ..) - фази на променлив състав; хомогенност диапазон за б -Ag2 S
33.31 - 33.33 ч. % S (177 ° С) до ж -Ag2 S - 32,36 - 37,04% S атом (727 ° С) .. Почти не разтворимост. във водата. орг. р-celeration, воден разтвор на амоняк. разлага воден р-избран KCN или царска вода. При загряване. във вакуум и се дисоциира в Agtv двойка S, Ур зададена температура зависимост от налягането на парите на S LGP = (mm Hg.) -. 13082 / T + 9.24. При загряване. окислява във въздуха, а -Ag2 S-полупроводник; фоточувствителна; електрон мобилността на 63.5 cm 2 / (V · е), дупките 19.0 cm 2 / (V · S); R 1000 ома · cm; коефициенти. thermopower -1000 тУ / K; топлопроводност 7,52 W / (см · К). б -Ag2 S г е 10 ома -3 · cm; коефициенти. thermopower - 60 тУ / К.
С erebra сулфид се среща естествено като минерали acanthite на -Ag2 S и аргентита б -Ag2 S.
С erebra сулфид Получава взаимодействие. Ag с S или евакуиран. кварцови ампули или р-ТА се стопяват. твърди Ag или S пари или пара поток S в Ar, N2. сероводород и утаяване на р-ра воден AgNO3.
-soed сребърни сложни сулфиди. Сулфидите, AG2 S в As, Sb, Bi, Si, Ge, Ga, In, и др. Naib. важно от тях tritioantimonat AG3 SbS3 (тъмно кафяви кристали) и tritioarse напрегнати AG3 AsS3 (червени кристали); не Сол. във вода и орг. р-celeration; получен чрез сливане с AG2 S Sb2 S3 (или AS2 S3) или с S Ag и Sb (As). Тя се среща естествено като минерали pyrargyrite AG3 SbS3 proustite и AG3 AsS3.
AG2 S се използва като компонент на твърдия електролит. полупроводникови материали. за да се утаи Ag + от р-рова; AG3 SbS3 и AG3 AsS3 - electrooptic материали. и elektroakustich. устройства. Ore. съдържащ acanthite, аргентита, proustite, pyrargyrite, суровина за получаване на Ag.

Свързани статии
