Медта е елемент от четвъртия период на единадесетата група на съответните елементи на масата. Медта в обикновен поглед - пластмасов материал преходен розово или златист оттенък.
Медта е един от най-много първо място на човешки материали, поради ниската температура на топене и маса наличността. Този материал обхваща седем метали, все още отглеждани в древни времена. Медта се появява като късове често от желязо, сребро или злато. Химическото наименование за мед - мед, настъпили от името на остров Кипър.
Таблица специфичното тегло на мед
Тъй като мед е труден материал, за да се изчисли делът му в областта на мира не е възможно. Тези изчисления се извършват в специални химически лаборатории. Въпреки това, средният специфичното тегло на мед е известен и варират от 8,63 до 8,8 г / см3.
За провеждане на изчисляването на теглото на мед и за опростяване на изчисленията по-долу е таблица със стойности на специфичното тегло и такива параметри като мед по тегло, в зависимост от единици за изчисление.
Специфично тегло и теглото на 1 м3 на мед в зависимост от единиците
От 8630-8800
свойства на мед
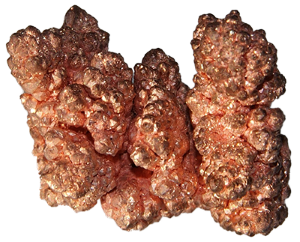
Медта е метал с сферографитен тип розово или златист оттенък. При взаимодействие с въздуха е покрита с филм оксид като червен или жълт оттенък когато овоскопирани - синьо-зелено цвят.
Този тип материал, заедно с цезиев, злато и осмий, е метал, който има цвят оцветяване изрично тип, характеризиращ се с сребристо сив или други метали. Мед образува лице центрирана кубична тип решетка.
Този материал има отлична електрическа проводимост, на второ място в този параметър след сребро и топлопроводимост. Медта има висок температурен коефициент на съпротивление, което е слабо зависи от температурата. Медта принадлежи към групата на диамагнитно.
Медта се използва в състава на цинк и мед сплави, калай и мед, никел, сребро никел, както и някои други.
Този елемент не е изложен на въздух в отсъствието на въглероден диоксид и влага. Мед - е слаб редуциращ агент не реагира с разредена солна киселина и вода. Той преминава в разтвор тип неокислително киселина или хидрат на амоняк с кислород, и калиев цианид. Добър окислява чрез взаимодействие с азотна киселина и сярна киселина, кислород, халогените, неметални оксиди, халогени и царска вода. При нагряване, той реагира с водородни халиди.
Медта се използва широко от древни времена. Неговите отличителни черти са все още сред най-добрите, което от своя страна прави мед един от най-популярните използваните материали. От основните приложения е да се осигури:
Свързани статии
