В групата на леки метали с плътност по-малко от 5 г / см, включва Al, Mg, Ti, Be, Са, В, Zn, К и други. Най-голямото промишленото приложение на тях са алуминий, магнезий, титан.
Алуминият е най-разпространеният метал в земната кора. Той се среща предимно под формата на съединения с кислород и силиций алуминосиликати. За използване на алуминий руда, богати на алуминий AI2O3. В повечето боксит се използва, който съдържа,%: 40-60 Al2 О3, Fe2 О3 15-30, SiO2 5-15, TiO2 2-4 и 10-15 хидрат влага.
Метод алуминиев производствен процес се състои от три етапа: извличане на алуминий от алуминиева руда, електролиза на стопен алуминий за да се получи първичен алуминий и рафиниране. Екстрахира се двуалуминиев триокис обикновено произвеждат алкален метод се прилага в два варианта: мокър (метод Bayer) и сух.
В мокър метод, боксит се суши, пулверизира и зарежда в автоклава, запечатани със силна основа, която се поддържа в продължение на 2-3 часа при температура от 150 ... 250 ° С и налягания до 3 МРа. В този случай се процедира взаимодействие на алуминиев хидроксид с натриев хидроксид:
Разтвор на натриев алуминат • Na2 О А12 О под формата на гореща маса се обработва по-нататък. Оксиди на желязо, титан и други примеси са неразтворими в основи, утаяване-суспензия.
Силициевият диоксид също така взаимодейства с основа, за да се образува натриев силикат: SiO2 + 2NaOH = О Na2 • SiO2 + 4H2 О, които от своя страна, взаимодейства с натриев алуминат утаява образуване неразтворимо съединение Na2 О · AI2 О3 · 2SiO2 · 2Н2 О ,
Месото, след филтруване и вода разреждане се оттича в ямката, където алуминат разтвор за да се утаи алуминиев хидроксид:
Алуминиевият хидроксид се филтрува и се калцинира при температура до 1200 ° С във въртяща тръбна пещ. Резултатът е алуминиев:
Алкална сух метод или метод синтероване се състои от ко-калцинира при температура от 1200 ... 1300 ° С смес от боксит, вар и сода, което води до образуване на утайка, която съдържа разтворим натриев алуминат:
Lime се консумира във формирането на неразтворими във вода калциев силикат, СаО • SiO2. Натриев алуминат се излугва с топла вода от утайката и полученият разтвор се продухва с въглероден диоксид:
Утайката се промива и се калцинира до получаване на алуминиев окис, както в предишния метод.
Алуминиеви произведени чрез електролиза на алуминиев разтваря в стопен криолит Na3 AlF6. Този метод е предложен през 1886 г., както в САЩ и P.Eru Ch.Hollom във Франция и все още се използва почти без промяна. Криолит се получава чрез интер-действие на HF флуороводородна киселина с алуминиев хидроксид, последвано от неутрализация с газирана кипене: 6HF + А1 (ОН) 3 = H3 AlF6 Zn2 + О;
Електролизата се провежда в алуминиево-електролитна баня, чиято схема е показана на Фиг. 2.5.
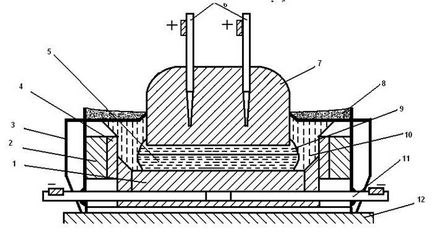
Фиг. 2.5. Схема електролитна клетка за производството на алуминий:
1 - катод въглища Blo-ки; 2 - огнеупорна облицовка; 3 - стоманена обшивка; 4 - въглерод плоча; 5 - течност алумино-ЛИЗАЦИЯ; 6 - метални пръти с гуми; 7 - въглероден анод; 8 - алуминий; 9 - Течен електрон-Debye-; 10 - кора на втвърден електролит; 11 - катодна текущата сумиране автобус; 12 - фундамент
Банята има стоманена обвивка с правоъгълна форма и неговата стена и огнището е направен от въглеродни блокове, изолирани с шамотни тухли. Облицовката на огнище монтирана стоманена катод автобуса, което позволява камерата въглища вана е катод на клетката. Söderberg аноди са вертикално разположени въглеродни електроди, потопени в стопилката. В аноди електролиза постепенно да изгори и да се премести надолу. Тъй като те са изградени върху изгарянето на масата анодната течност, от което летливите вещества се отстраняват чрез нагряване и се поставя своята коксуване. Електролитът се загрява до работната температура 930-950 ° С Алуминий, консуматив при електролиза, периодично се зарежда в банята от по-горе. се формира на охлаждащия въздух на повърхността на електролит кора. На страничната повърхност на банята, образуван от втвърдяване електролитен слой (черепа), системата за предварително сигурна защита предотвратява облицовката от разграждане и топлоизолационен баня. При висока температура алуминиев AI2 О3. разтворен в електролита, дисоциира в йони: A12 О3 = 2А1 3+ + O 2- върху повърхността на огнището на въглища, което е катода, метални йони се редуцират до: 2AL 3+ + 6e = 2AL
Чрез намаляване на съдържанието на алуминий в електролита периодично се зарежда в своята електролитна баня. Течен алуминиев натрупва на огнището на клетката и периодично се отстранява чрез вакуум кофата.
Кислород йони се заустват в анода на въглерод: 3O 2- 6e = 3 / 2O2. анод е окислен за образуване на СО и СО2. са отстранени вентилационни устройства. Електролиза клетки, свързани последователно в поредица от бани 100-200.
Основно алуминий се произвежда в електролитната клетка е замърсена от примеси Si, Fe, неметални включвания (AI2 О3, С), както и газове, за предпочитане водород. За пречистване се подлага на рафиниране алуминиева или хлориране, или обезмаслено електролитен метод.
А чист алуминий се получава чрез електролитно рафиниране, където електролита е безводен хлорид и флуоридни соли. Стопеният алуминий подлага на електролит и електролиза анодно разтваряне. , Получени чрез електролиза чистота рафиниране алуминий до 99,996% консумираната електроенергия, химическата и хранително-вкусовата промишленост. Още по-чист алуминий (99,9999%) може да бъде получено чрез топене зона. Този метод е по-скъпо от електролиза, малки производители и се използва за производство
малки количества метал в случаите, когато се изисква висока степен на чистота, например за производството на полупроводници.
Свързани статии
