Проблемът за лечение на тежки вътреболничните инфекции
резистентност флора
Устойчивост на нозокомиални инфекции с антибиотици (AB) е важна причина влияние върху консумацията на ресурси и смъртност [1]. Бързият растеж и разпространение на резистентност към AB болница флора се наблюдава в целия свят, но този процес е неравномерно. Грам-отрицателни и грам-положителни организми са основни патогени на нозокомиални инфекции [2-5]. Най-проблемни микроорганизми са метицилин резистентни S.aureus (MRSA) и грам-отрицателни бактерии - производители на β-лактамаза с разширен спектър (ESBLs), тъй като те притежават резистентност към много AB [6-11].
Интензивно отделение (ICU) са най-подходящите служби по отношение на появата на резистентни организми на AB. Това се дължи на няколко причини: 1) висока честота на неефективно начална терапия и продължителна употреба на широк спектър AB; 2) концентрацията на най-тежките пациентите пушачите на сравнително малка площ; 3) ниски икономически интереси помощен медицински персонал в обучение и практикуване на метода за ограничаване на разпространението на устойчиви контакти флора; 4) увеличаване на броя на хоспитализирани пациенти с остри и хронични заболявания, изискващи продължително лечение и са източник на бактерии устойчиви на AB [1, 12-13].
Преодоляване на устойчивост на AB
Идеалният антимикробна терапия трябва да осигури адекватна (активен срещу избран патоген) започване на лечението и ограничаване на растежа и разпространението на резистентност. Сравнително наскоро, основната идея на тази програма беше представена под формата на 12 принципи за предотвратяването на съпротива в болницата. Един от ключовите елементи на тази програма е да участва в решаването на проблемите на експертите в тази област (инфекциозно заболяване, клиничните епидемиолози, микробиолози, клинична фармакология), особено при разработването на методи за оптимизиране на лечението и да ограничи резистентността към AB.
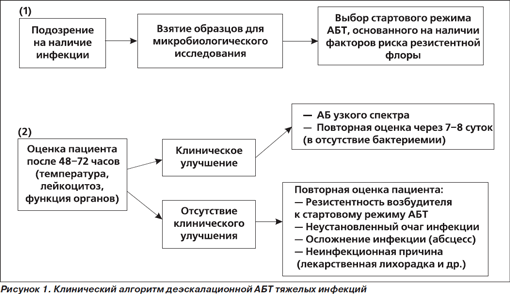
1. Предполага се, че присъствието на тежки вътреболнични инфекции.
2. Оценка на пилотния режим, след като получи ABT микробиологичните данни.
3. Приключване на ABT на курса - непрекъснат мониторинг.
Устойчивост AB: рискови фактори и тяхното влияние върху резултатите
Рисковите фактори за появата на резистентност към AB
AB стимулира появата на резистентност, както и мерки, насочени към ограничаване на използването им, са пряко свързани с устойчивостта на ограничение. Много изследвания са установили тясна връзка между използването на акумулаторна батерия и появата на бактериална резистентност към нея [15-17]. Има и други рискови фактори за развитието на резистентност към AB: продължителна хоспитализация; използване на инвазивни устройства (ендотрахеална тръби, съдови катетри), вероятно поради образуването на биофилм върху повърхностите на тези устройства; живеещи в домове за хора с увреждания и възрастните хора; неефективни мерки за контрол на инфекция [13].
Появата на нови щамове на патогени в общността води до проникване на резистентни микроорганизми в болницата. Сравнително наскоро доказано безопасни появата и разпространението на щама на S.aureus, оксацилин-резистентни (CA-MRSA) [17-20]. Продължителната употреба на AB е най-важният фактор за появата на резистентност към него, и този ефект може да бъде значително отслабена звук ABT [21-22].
Последиците от неадекватното ABT
Увеличаването на смъртността. Показано е, че емпирично антимикробна терапия на тежки инфекции лекарства неактивни срещу патогени, т.е. неадекватна започне ABT, води до значително увеличение на смъртността - около 2 пъти. Неотдавна, подобни данни са получени при пациенти със сепсис [23-31]. Промяна на ABT животозастрашаващи инфекции, след получаване на микробиологична проучване данните не подобрява значително резултатите от лечението поради настъпването на тежки усложнения: септичен шок, кръвоизливи и други причини [24, 26]. В тези проучвания е показано, че съпротивлението на растеж болница флора води до увеличаване на смъртността поради ниската ефективност на стандартни емпирични режими ABT. Наскоро препоръките на American Thoracic Society и Дружеството на инфекциозно заболяване (ATS / IDSA) за лечение на нозокомиална пневмония бе подчертано значението на посредствено антимикробна терапия като причина за растежа на смъртност в болница [32]. Тези насоки подчертават значението на: 1) наблюдения върху чувствителността на местната флора AB (непрекъснато актуализиране на данни за всички болници и индивидуален ICU за да се гарантира качеството на избора на емпирични режими антимикробна терапия); 2) правилното дозиране AB (за оптимизиране тъканни концентрации).
Увеличението на разходите. По принцип увеличава разходите, свързани с нозокомиални инфекции, които обикновено са причинени от резистентни към флора AB [17, 33]. Установено е, че инфекции, причинени от MRSA, в сравнение с инфекции, причинени от чувствителни към метицилин / оксацилин S.aureus (MSSA), са отговорни за по-висока смъртност. В мета-анализ на 30 проучвания е показано, че MRSA-бактериемия, независимо от други фактори увеличават риска от смърт [34]. При оценката на смъртността MRSA атрибут и MSSA разлика е около 25% [35]. Причините за тези различия се смята, че: 1) тежестта на инфекцията; 2) да използват емпирични ABT недостатъчни. Обикновено, пациенти с инфекции, причинени от MRSA, посочени по-тежко протичане на заболяването и по време на приемане в болница, и по време на диагностициране на инфекция. В допълнение, пациентите, нуждаещи се от продължително болнично лечение.
Фактори, влияещи върху избора на изходните ABT
Адекватна режим ABT. При определяне на режим на емпирична антимикробна терапия трябва да се счита за най-важният фактор на 4: 1) присъствието на инфекция (или се подозира диагноза на инфекциозни заболявания); 2) вероятност етиологичен значението на някои патогени в някои видове нозокомиални инфекции (вътреболнични инфекции етиологичната структура); 3) спектър на микроби циркулиращи в съоръжението, и по-специално тяхната устойчивост към антибиотици (мониторинг на местната флора); 4), ако пациентът има рискови фактори за инфекция, причинена от резистентни микроорганизми. В идеалния случай трябва да се вземат под внимание всички фактори, посочени по-горе.
Наличието на инфекция. Много критични състояния, придружени от общи възпалителни реакции, клинични и лабораторни признаци, които не се различават съществено от признаци на инфекция. В случаи на хоспитализирани пациенти в ОИТ незаразните заболявания признаци на инфекция (основен фокус, признаци на системна инфекция, повишени нива на цитокини, остри фазови протеини, прокалцитонин) обикновено не причинява диагностични затруднения. Въпреки това, в тежка polytrauma, изгаряне токсемия, разрушително панкреатит, следоперативни хирургически инфекциозните усложнения, полиорганна недостатъчност възниква генерализирана възпаление, което често създава значителни диференциални диагностични трудности при премахване на вътреболнични инфекции и води до значително увеличаване на използването на антимикробни средства, включително широк спектър.
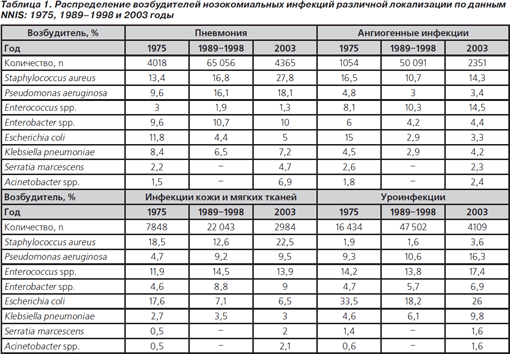
Увеличаването на броя и съпротивление на грам-отрицателни бактерии без ферментиране. Един от най-важните тенденции е нарастващата значимост на Acinetobacter SPP. при пациенти с uroinfektsiyami, пневмония и навити хирургични инфекции [39-41]. Въпреки atsinetobaktery ниския относителен принос (
Мониторинг на местната флора и съпротивата AB
Влиянието на други фактори, включително механична вентилация. Разпространението на мултирезистентни флора варира значително в зависимост от патологията на пациентите, като болници и офиси. Мултирезистентни патогени най-често се отличават от тежки пациенти, пациенти с хронични заболявания като пневмония с наличието на рискови фактори, свързани с медицински грижи (таблица. 2) и пациенти с късно нозокомиална пневмония. NPivl рискови фактори, причинени от мултирезистентни флора е изследвана при 135 пациенти, които са на механична вентилация [17]. Продължителността на механична вентилация преди пневмония и по-рано среща AB (в рамките на 15 дни преди датата на NPivl) са значими рискови фактори за NPivl, причинени от резистентни микроорганизми. В края NPivl (настъпили след 5 дни на ендотрахеална интубация) при пациенти, лекувани преди AB, причинени от мултирезистентни флора обикновено е: P.aeruginosa. Acinetobacter baumannii, Stenotrophomonas малцорШИа. MRSA. Тези данни отново показват необходимостта от по-рационално използване на АВ при пациенти, подложени на механична вентилация, както и за сметка на преди антибиотична терапия като основен рисков фактор NPivl причинени от мултирезистентни флора. Същата нужда се определя от избора на режим NPivl емпирична терапия (докато резултатите от микробиологично изследване) широкоспектърни препарати, които могат да преодолеят важни известни механизми на резистентност нозокомиални флора за подобряване на адекватността на емпиричната режим ABT.

Различията болнични флора в различни ICU една болница
Изследване посветена на изследването на различни мултирезистентни патогени в различни ICU единична болница. [44] Значителни разлики в чувствителността на патогени в хирургически, травма и обща ICU. Намерено ниска чувствителност на Acinetobacter SPP. на имипенем в хирургично и висока чувствителност в ОИТ на травма. Подобни наблюдения са направени и в други страни в ОИТ [45, 46]. Тези данни подкрепят необходимостта от хармонизиране на общи препоръки за антимикробна терапия и местни данни относно чувствителността (в страната, града, болницата и отделение за интензивно лечение). Това помага да се вземат под внимание специфичните грам-отрицателни флора, като разпределение честота производство β-лактамаза с разширен спектър между K.pneumoniae или E.coli; устойчиви на флуорохинолони P.aeruginosa. резистентни към карбапенеми A.baumannii. С висока степен на вероятност от инфекции, причинени от тези патогени, че е необходимо да се внесат поправки емпирични режими терапия.
Особено пациенти, които са в състояние да влияят на устойчивостта на флората AB
В допълнение към местните или регионалните характеристики на флората, има много характеристики на пациентите, които увеличават вероятността за селекция на резистентни флора. Ето защо изборът на емпирично лечение трябва да се основава на данните от мониторинга на местната флора, като се вземат предвид характеристиките на пациентите. При наличие на рискови фактори за развитие на инфекции, причинени от болничните щамове на S.aureus. P.aeruginosa. Acinetobacter SPP. поради високата вероятността за устойчивост значително увеличава смъртността [47-51]. Инфекции, причинени от резистентни флора обикновено се появяват при хоспитализирани пациенти с продължително лечение в болница, дълго съдова катетеризация, използването на антибиотици, присъствието на рани от залежаване, хирургични рани инфекции, ентерално хранене и хемодиализа.
Разпространението на нозокомиалните флора в болница
Някои видове медицински грижи, като диализа, химиотерапия, хирургични болници да ги доведе до увеличаване на броя на пациентите, които получават лечение в болнична среда [52]. Пневмония и ангиогенни инфекции, свързани с медицинско обслужване, често се класифицира като придобити в обществото инфекции, и първоначално лекувани със съответните препоръки. Въпреки това, честото общуване между пациенти и здравни специалисти, които работят в болници, в резултат на факта, че колонизищи флора при тези пациенти започва да се различава от придобита в обществото, и се превръща по-скоро като вътреболнична. Например, MRSA, изолиран от инфектирани пациенти в болница, амбулаторно значително различни от и имат различна чувствителност към AB [19].
В допълнение, през последното десетилетие има значителна промяна в съпротивлението на придобити в обществото флора. Streptococcus пневмония е основен причинител на придобита в обществото пневмония, но инфекцията е причинена, и други патогени (Chlamydia пневмония. Mycoplasma пневмония. Acinetobacter SPP. MRSA, Legionella SPP.), Разпространението на която се различава значително в различните региони и продължава да се променя [42, 53, 63, 81 ]. Разпространението на резистентност към патогени AB-болнични инфекции значително усложнява тяхното лечение изисква промяна в съответствие с микробиологични и епидемиологични данни [54]. Всичко това води до необходимостта да се разделят на инфекции, свързани с медицинско обслужване, от инфекции, които традиционно се приписват на придобита в обществото [17, 32, 55, 56].
заключение
устойчивост на растежа AB е основен проблем за ефективното прилагане на клиничната AB. Сложността на поддържане на баланс между необходимостта от подходяща антимикробна терапия и ограничаване на растежа на устойчивост на флора диктува необходимостта от нови подходи за стратегията на използване на батерията. Въпреки факта, че новата КБ разшири възможностите за лечение, създаването им не могат да бъдат в крак с развитието на резистентност флора. Ако в момента на релевантността на грам-положителни патогени е достъпно лекарства, които да решават всички проблеми на резистентност срещу грам-отрицателни бактерии, такива препарати за локално приложение там. Това отново подчертава значението на стратегическото мислене при кандидатстване AB в клинични условия може да доведе до баланс между ефективността на използването им и ограничаване на растежа на съпротива патогени.
Свързани статии
