Решени като система от уравнения, ние откриваме, неизвестен N1 и N2:
Изразяване във формулите стойности в SI единици, замествайки с техните стойности, изпълняват изчисления, получаваме
1.2. вътрешна енергия и топлинна мощност на идеален газ
Vnutrennyayaenergiyagaza сума от енергията на отделните молекули. В едно Kmol на всички газови молекули, съдържащи се NA (NA Авогадро --chislo). Следователно един kilomole идеален газ има вътрешна енергия, равна
Вътрешният енергия за произволна газ маса m:
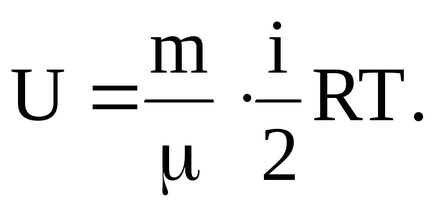
където - моларната маса на газа.
Специфичен топлинен капацитет "в" на газ се нарича физична величина, която е числено ravnayakolichestvu топлина, която трябва да бъде съобщено, че един от масата на газ да се загрява с един градус.
Моларен топлинен капацитет "С" се нарича физическа величина, която е числено равно на количеството топлина, което трябва да се докладва за един мол от газ да се увеличи температурата от една степен.
Комуникацията между специфичната и моларен топлинен капацитет:
Моларното специфичната топлина при постоянен обем "Cv" - физическа величина е числено равно на количеството топлина, което трябва да се докладва за един мол от газ да се увеличи температурата от една степен в постоянен обем.
Моларното специфичната топлина при постоянно налягане "Ср" - физическа величина е числено равно на количеството топлина, което трябва да се докладва за един мол от газ да се увеличи температурата от една степен в условията на постоянно налягане.
Ако газът се загрява при постоянен обем, газа, доставян на топлината idotna увеличи своя вътрешна енергия. Следователно в този случай промяната на вътрешната енергия на газа го prinagrevanii един градус е равен molyarnoyteploomkosti
Когато загрява в molyagaza usloviyahpostoyannogo налягане, което му предава външната топлина е не само да се увеличи неговата вътрешна енергия, но също така и за извършване на работа срещу външни сили.
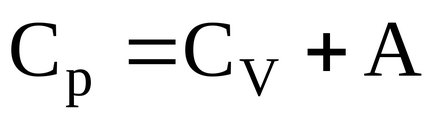
В работата на разширяване на един мол от газ под постоянно налягане
където R - универсална константа газ.
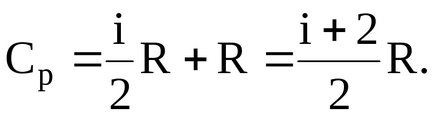
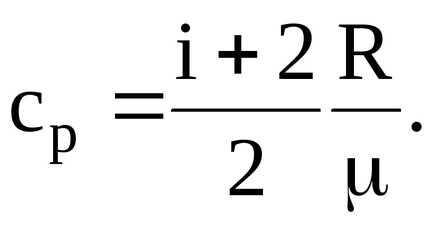
1.2. Примери за решаване на проблеми
1.2.1. Изчислява специфичните топлини при постоянно налягане и при постоянен обем неон и водород носещи газове за идеал.
Решение. Между моларен и специфичната топлина на идеалния газ при постоянно налягане и при постоянен обем има връзка:
По този начин, за udelnyhteploemkostey имаме:
Знаейки, че неон odnoatomnyygaz dlyanego степени на свобода и = 3, = 2010 -3 кг / мол, и водороден газ за нея двувалентни степени на свобода и = 5, = 2710 -3 кг / мол. Заместването на всяка от горните формули записва стойност и стойността на универсалната газова константа R = 8,31 J / (molK) за изчисляване на специфичната топлина:
.
1.2.2. Виж отношението на специфични топлини при постоянно налягане и постоянен кислород обем.
Решение. Съотношението на специфични топлини на постоянно налягане и постоянен обем на идеалния газ е равна на молно съотношение на специфични топлини на постоянно налягане и постоянен обем:
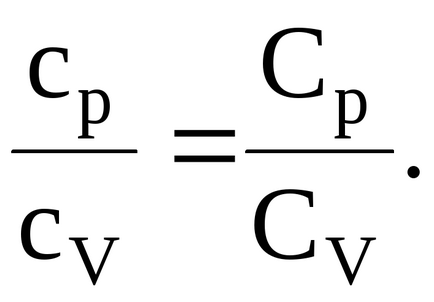
Знаейки, че моларното специфичната топлина при постоянно налягане и при постоянен обем, свързан с броя на степените на свобода и са
За отношението на специфични топлини ще
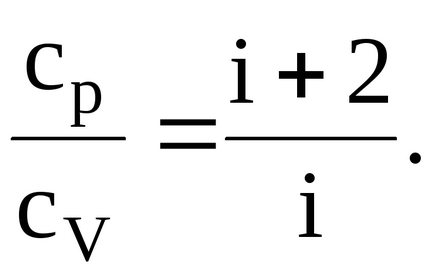
Кислород на двуатомен газ, следователно, броят на степените на свобода I = 5. Заместването аз ценя vyshezapisannuyu формула, ние имаме:
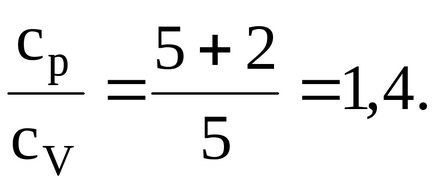
1.2.3. Специфична топлина на двуатомен газ е 14,7 кДж / (kgK). Намери моларната маса на газа.
Решение. Известно е, че специфичната топлина при постоянно налягане моларен специфична топлина, свързани с газ:
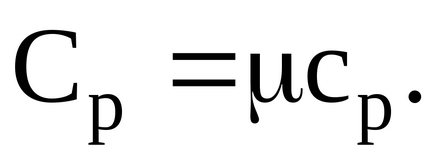
Моларното специфичната топлина при постоянно налягане
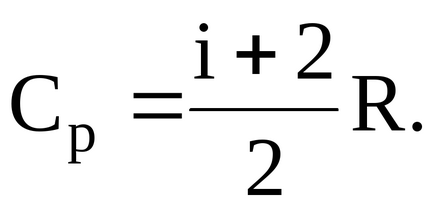
където I - броят на степените на свобода на газа.
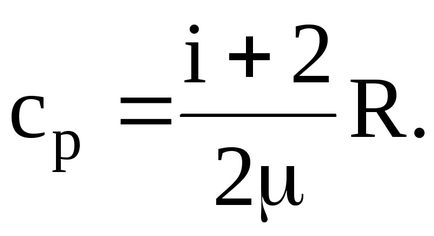
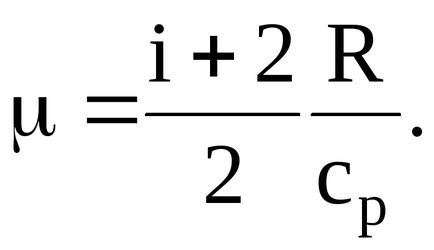
Podstavlyayav формула получава стойности на данни в количествата на проблема с държи сметка за факта, че за една молекула, газ и = 5, имаме:
1.2.4. Изчислява специфичната топлина при постоянен обем и постоянно налягане, смес от неон и водород, при масова част на неон и водород представлява 1 = 80% и 2 = 20%, съответно. Специфичната топлина капацитет за неон CV = 6,2410 2 J / (kgK) ср == 1,0410 3 J / (kgK); за водород-CV = 1,0410 4 J / (kgK) ср = = 1,4610 4 J / (kgK).
Решение. Като цяло, количеството топлина, необходима за нагряване на смес от газове, например, чрез нагряване в постоянен обем от температура Т1 до температура Т2 равен на:
където CV (см) - специфичен топлинен капацитет на сместа;
(Т2 -T1) - промяна в температурата.
От друга страна, това количество топлина може да бъде vychislenopo формула:
където Q1 и Q1 - съответно количеството топлина, което трябва да бъде
докладва за промяна на температурата на неон и водород поотделно;
CV1 и SV2 - специфичен топлинен капацитет на неон и водород при постоянен обем;
М1 и М2 - маса на неон и водород.
По този начин ние имаме:
където
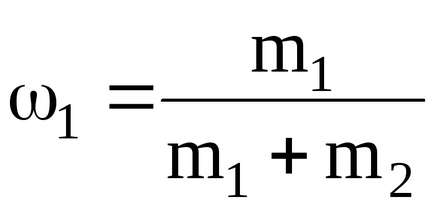
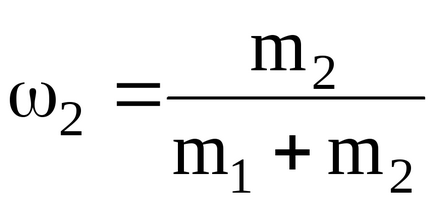
Podstavlyayachislennye стойности за udelnoyteploemkosti смес ivodoroda неон в postoyannomdavlenii, budemimet:
Аналогично може да се получи формула за определяне на специфична топлина капацитет на сместа от неон и водород при постоянно налягане:
Заместването на цифровите стойности за специфичната топлина при постоянно налягане на сместа, имаме:
1.2.5. Кислород 2 кг заема обем V1 а = 1 m3 и p1 налягане = 0,2 МРа. Газ се нагрява при първо при постоянно налягане до обем V2 = 3. 3 m и след това при постоянен обем на p3 налягане = 0,5 МРа. Намери промяната във вътрешната енергия на газа.
Решение. Промяна на вътрешния енергиен на газа
където CV = МР / 2 - специфична топлина при постоянен обем;
- моларната маса на газа;
T = (Т2 - Т1) - промяна на температурата на газа в последните и първоначални състояния;
I = 5 - брой степени на свобода (двуатомен кислород газ).
Температурата на газа в началните и крайните страни могат да се определят от уравнението Менделеев-Clapeyron
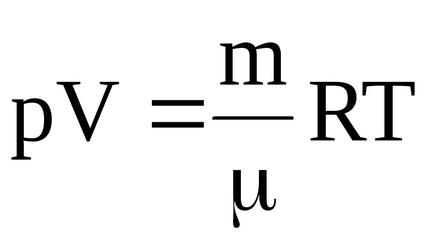
За първоначална температура
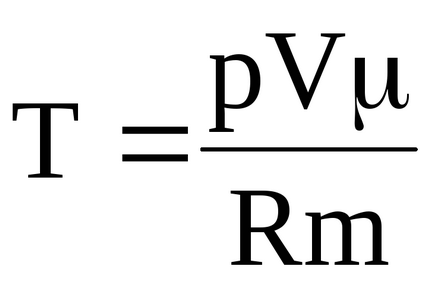
За ограничен температура
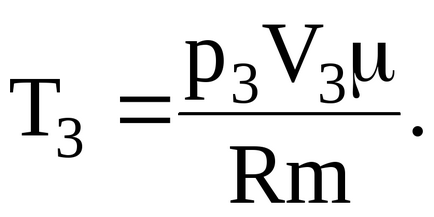
След това променете vnutrenneyenergiigaza
Podstavlyayachislennye ценности, които имаме
1.2.6. Маса m = 10 грама на кислород е р налягане = 0,3 МРа и температура 10 ° С След нагряване под постоянно налягане на газа се V2 = обем от 10 литра. Виж количеството топлина Q, полученият газ и топлинна енергия движение на газови молекули W преди и след нагряване.
Решение. Количеството топлина Q, полученият газ по време на нагряването
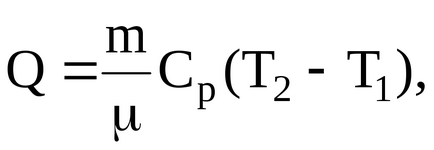
където
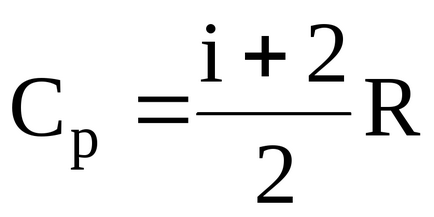
I = 5 - брой степени на свобода (двуатомен кислород газ);
R = 8,31 J / (mol7K) - универсална постоянен газ;
= 0032 кг / мол, - молекулното тегло на кислород;
Т1 и Т2 - температура на газа в началните и крайните страни. За да се определи температурата на газа в крайното състояние на използване връзката между температурата и обема на газ, нагрява под постоянно налягане:
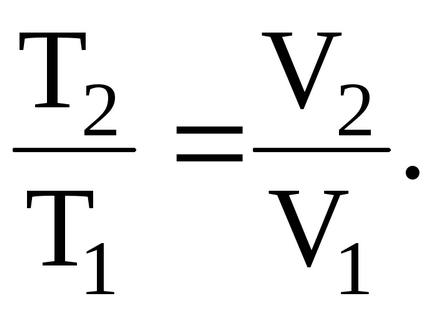
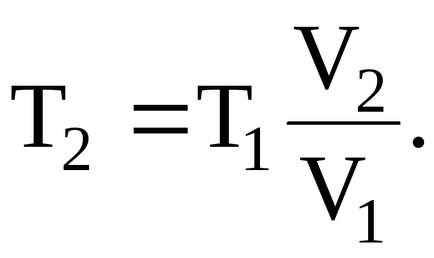
С помощта на уравнението на Менделеев-Клапейрон уравнение:
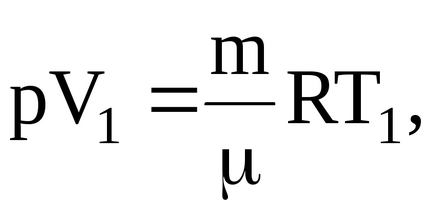
nahodimobem газ в първоначалното състояние:
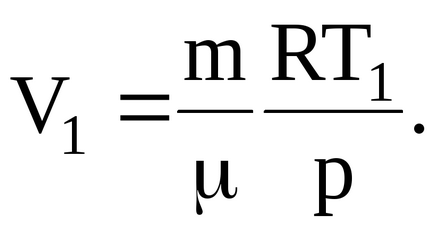
Ние ще имаме съотношение на крайната температура:
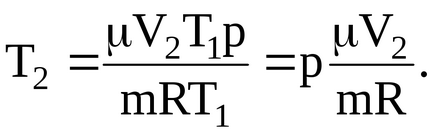
Заместващите числени стойности определящи крайната температура на газа:
Podstavlyayachislennye стойност е количеството топлина, произведено в технологичния газ нагряване:
Топлинната енергия движение на газови молекули могат opredelitpo формула
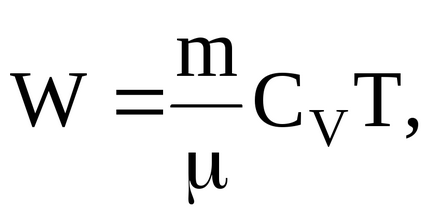
където CV = МР / 2 - моларен топлинен капацитет на газ при постоянен обем.
По този начин, топлинната енергия на движение на молекулите на газа в първоначалното състояние, имаме:
в крайното състояние:
.
1.2.7. Кислород 2 кг заема обем V1 а = 1 m 3 и p1 налягане = 0,2 МРа. Газ се нагрява при първо при постоянно налягане до обем V2 = 3. 3 m и след това при постоянен обем на p3 налягане = 0,5 МРа. Намери промяната във вътрешната енергия на газа, те работят перфектно и топлина се предава на газ.
Решение. Известно е, че промяна на вътрешната енергия на газа пропорционално на температурата на климата,
От уравнение Менделеев-Клапейрон
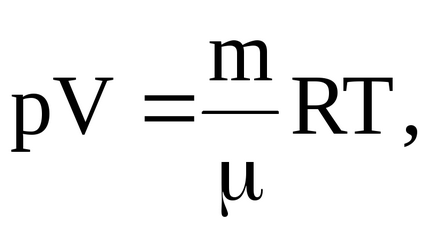
Можете да определите температура характеристика на съответните държави:
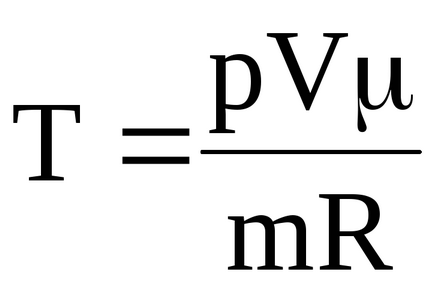
Следователно, температурата на газа в първоначалното състояние
Следователно, за да се промени на вътрешната енергия на газа в своя преход от първоначалното състояние на крайното състояние, ние имаме:
В движи извършва газ работа
където А1 - газ работа, извършена при прехода към условията на постоянно налягане;
A2 - газ и се извършва при прехода в условията на постоянен обем.
Газ извършената работа при преминаване към постоянни условия за налягането, определено от съотношението:
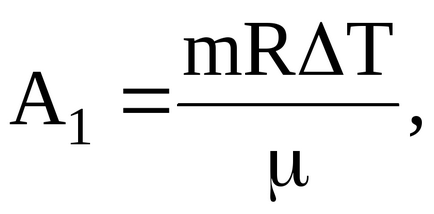
газ и извършената работа по време на прехода в постоянен обем:
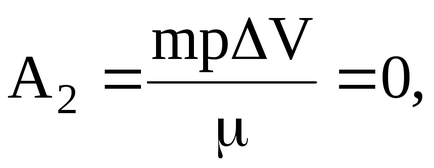
По този начин, в този случай
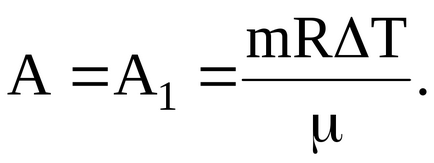
Количеството топлина, прехвърлени на газа е равна на стойността на промяната в неговата вътрешна енергия и извършената от тях работа,
След проверка на размера и заместване на числени стойности, ние имаме
Т1 = 0,210 6 13210 -3 / 8,3110 3 2 = 385 К;
Т2 = 0,210 6 33210 -3 / 8,3110 3 2 = 1155 К;
Т3 = 0,510 6 33210 -3 / 8,3110 3 2 = 2888 К;
U = 528,31 (2888-385) / 23210 -3 = 3,2510 3 J;
А = 28,31 (1155-385) / 3210 -3 = 0,410 3 J;
Q = 3,2510 + 0,410 3 3 3 J = 3,6510.
1.2.8. Тегло 12гр азот е в затворения съд на обем
V = L 2 при Т = 10 о S.Posle нагряване на налягането в съда е равна р = 1,33 МРа. Какво количество топлина Q съобщава газ при нагряване?
Решение. Тъй като обемът на газа не се е променило, посланието е количеството топлина, той отиде да промени вътрешната енергия
което от своя страна може да се определя като:
където Cv = МР / 2 - моларен специфична топлина при постоянен обем от азот.
За определяне на крайната температура Т използва факта, че prinagrevanii на газ под постоянно съотношение пропорционален обем налягане до съотношението на температурата в началните и крайните страни P1 / p2 = T1 / T2.
Nachalnoe налягане определя от уравнението Менделеев-Clapeyron записва на първоначалното състояние:
Тъй като хипотеза проблем V1 = V1 = V, тогава имаме за крайната температура:
Заместването на стойността на Т2 в промяната на формула на вътрешната енергия, което е равно на количеството топлина-Отчетените газ накрая получаване на:
Размерността на резултатите е очевидно. Цифровата стойност на Q е равно на
Q = 4,1310 3 J = 4.13 кДж.
1.2.9. работен обем V на = 20 л кислород под налягане р = 100 атмосфери и температура от седем тон = О С се загрява до Т = 27 ° С, което количество топлина по този начин абсорбира газ?
Решение. Тъй като термично разширение коефициентите на твърди вещества е значително по-малък (около сто пъти), отколкото за газове, в условията на този проблем може да бъде игнориран и разглежда като продължение на изохорен процес на загряване газов цилиндър.
Когато изохорен процес, снабден със системата, количеството топлина, е да се промени вътрешната си енергия.
От дефиницията на моларен топлинен капацитет, следва, че начално количество топлина предава към тялото чрез увеличаване на температурата дТ, е равна на: DQ = CV DT.
Броят на моловете е намерена от уравнението на състоянието на газ (Менделеев-Clapeyron) = m / = p1 V / RT1.
Тъй като газът се загрява при постоянен обем, след това с = CV. където CV = МР / 2.
Заместването ценности автобиография и формулата за елементарните количества топлина, получаваме:
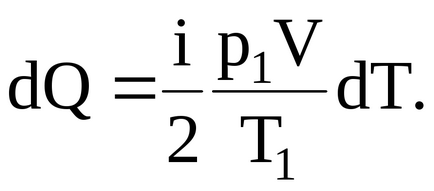
Следователно, интегриране и като се има предвид, че всички стойности на I, p1. T1. V - константа, ние откриваме, общото количество топлина абсорбира от газ при нагряване от Т1 до Т2. която е числено равна и ще izmeneniyuego вътрешна енергия:
След проверка на измерение чрез заместване на тази формула стойностите на количества, включени в системата SI, ние извършване на изчисления:
U = 59,810 5 210 -3 (300-280) / 2280 = 3510 3 J = 35 кДж.
Свързани статии
