Плътност на амоняк и други физични свойства
При нормални условия, амонякът е безцветен газ с остър задушаваща миризма. плътност амоняк е 0,73 кг / м3.
Амоняк молекула има химически състав, който се отразява от формула NH3. Той има формата на триъгълна пирамида (dNH = 0,10nm, HNH ъгъл 0 = 107.3) (Фиг. 1). Според валентна връзка теория отговаря SP 3 -hybridization валентността орбитали азотен атом. От четирите орбитите SP 3 -Hybrid три азотни участва в образуването на три а-връзки N-Н и четвъртата орбитала се свързващ електронна двойка. От гледна точка на метод на молекулните орбитали, това съответства на запълване три свързване и малко свързващи молекулярни сигма орбити:
Тъй като няма свързващ два електронен облак е ориентирана в пространството, молекула амоняк - изразена донор електронна двойка и има висока полярност (т = 0.49 х 10 -29 m х Cl).
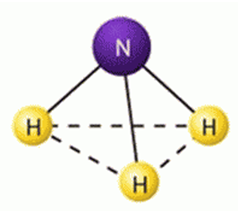
Фиг. 1. Структура на молекулата на амоняк.
Полярността на N-H връзки между молекулите на амоняк води водородна връзка. Следователно, точката на топене (-77,8 ° С) и точка на кипене (-33,4 ° С) амоняк доста висока; тя се характеризира с голяма специфична топлина на изпарение и лесно втечнен.
Течен амоняк като вода, - силно йонизиращо разтворител. Така производни на NH4 + в течен амоняк се държат като киселини (аминокиселини) и производни NH2 - - като база (ammonoosnovaniya). Например, силни киселини са в течен амоняк, на NH4CI, NH4 NO3. и бази - KNH2. Ба (NH2) 2. Digidronitridy Zn (NH2) 2. Al (NH2) 3 се държат като амфотерно съединение.
Амонякът е много разтворим във вода (при 20 ° С в обем от вода се разтваря приблизително 700 обема амоняк). Добра разтворимост поради образуването на водородни връзки между молекулите на NH3 и Н2 О.
Кратко описание химични свойства и плътност амоняк
Амонякът е силно реактивен, е склонен към реакции prisoedineniya.Sgoraet кислород реагира с киселини, метали, халогени, оксиди и халогениди.
2NH3 + 2AL = 2AlN + 3H2 (т = над 600 ° С).
Качествена реакция на амоняк - почерняване хартия, smochennoyrastvorom HG2 (NO3) 2 (образуване на живак). Сухи калциев оксид, амоняк.
Течен амоняк - основния протонен разтворител; и rastvoryaetseru халогениди (без флуорид) и нитрати на алкални метали, galogenidyammoniya, калиев перманганат; слабо разтваря неорганични флуориди, сулфати, карбонати.
Примери за решаване на проблеми
Изчислява се моларната маса на газа, който е плътността на въздуха е 0.756.
Съотношението на масата на газ към маса на друг газ, взето в същото количество при същата температура и същото налягане, се нарича относителната плътност на първия газ във втория. Тази стойност показва колко пъти първите количества газ са по-тежки или по-леки от втория газ.
Относителната молекулна маса на въздух взети равна на 29 (по отношение на съдържанието на азот във въздуха, кислород и други газове). Трябва да се отбележи, че терминът "относителна молекулна маса на въздух" се използва обикновено, тъй като въздухът - смес от газове.
Dair (газ) = М (газ) / M (въздух);
М (газ) = М (въздух) х Dair (газ);
M (газ) = 29 х 0756 = двадесет и два гр / мол.
Моларен маса на газ, равен на 22 гр / мол.
Определяне на моларната маса на неизвестен газ ако равни обеми газ и кислород при същите условия имат маси от 4,15 грама и 0.32гр
Съотношението на масата на газ към маса на друг газ, взето в същото количество при същата температура и същото налягане, се нарича относителната плътност на първия газ във втория. Тази стойност показва колко пъти първите количества газ са по-тежки или по-леки от втория газ.
Моларен маса е водород:
След това, моларната маса на неизвестен газ
М (газ) = М (О2) х DO2 (газ) = 32 х 1,328 = 42,5 г / мол.
Свързани статии
