Относно: митохондриалната респираторна верига. окислително фосфорилиране
1. Структура на митохондриалната респираторна верига, последователността на прехвърляне на протони и електрони. Формула водородни акцептори: NAD, FAD, KoQ. Роля на кислород във веригата на електронен транспорт.
2. ензимен комплекс на дихателната верига - състава, функция. Трансмембранен потенциал, неговото формиране и използване. Ролята на вътрешната митохондриална мембрана.
3. Концепцията на окислително фосфорилиране. скорост фосфорилиране (определение, изчисляване на пробата). Ролята на АТФ синтаза. Основните направления на използване на АТФ в клетката. ATP формула.
4. Енергиен баланс (добив АТР) активно окисляване ацетат (ацетил-СоА) и пируват.
5. не-фосфорилиране или свободни основи окисляване - биологична роля. Откачването на окисление и фосфорилиране в митохондриите.
6. Вещества, които влияят на процеса на окислително фосфорилиране в митохондриите: дишане инхибитори protonophores, йонофори.
Дихателната верига и окислително фосфорилиране.
14.1.1. Реакцията на пируват дехидрогеназа и цикъла на Кребс настъпва дехидрогениране (окисляване) на субстрати (пируват, изоцитрат, α-кетоглутарат, сукцинат, малат). В резултат от тези реакции произвеждат NADH и FADH 2. Тези намалени коензими се окисляват форма в митохондриалната респираторна верига. Окислението на NADH и FADH 2 течаща conjugately с синтеза на АТФ от АДФ и Н 3РО 4 се нарича окислително фосфорилиране.
Структурата на верига на митохондриите е показано на Фигура 14.1. Митохондриите са вътреклетъчни органел има две мембрани: външен (1) и вътрешен (2). вътрешната митохондриална мембрана образува множество гънки - Crista (3). Пространството, ограничена от вътрешната митохондриална мембрана, се нарича матрицата (4), в пространството, ограничено от външната и вътрешната мембрани - intermembrane пространство (5).
Фигура 14.1. Структурата на верига на митохондриите.
14.1.2. Дихателната верига - серия верига ензими извършва прехвърлянето на водородни йони и електрони чрез окисление на субстрати с молекулен кислород - крайния водороден акцептор. По време на тези реакции освобождаване на енергия се извършва постепенно, на малки порции, и тя може да се съхранява под формата на АТФ. Локализация на дихателната верига ензими - вътрешната митохондриална мембрана.
Дихателната верига се състои от четири мултиен комплекс (фигура 14.2).
Фигура 14.2. Ензимни комплекси на дихателната верига (означени с бизнес конюгиране на окисление и фосфорилиране):
I. NADH-KoQ-редуктаза (междинно съединение съдържа водородни акцептори: флавин мононуклеотид и желязо сяра протеини). II. Сукцинат-KoQ-редуктаза (междинно съединение съдържа водородни акцептори: FAD и желязо сяра протеини). III. KoQN 2 -tsitohrom в редуктаза (електронни акцептори включва: цитохроми б и желязо сяра протеини с 1.). IV. Цитохром с оксидазна (електронни акцептори включва: цитохроми един и 3. медни йони Си2 +).
14.1.3. В убихинон (коензим Q) действат като междинни носители на електрони и цитохром с.
Убихинон (KoQ) - мастноразтворими витамини като вещество, което е в състояние лесно да дифундира в хидрофобната фаза на вътрешната мембрана на митохондриите. Биологичната ролята на коензим Q - електронен транспорт в дихателната верига на флавопротеини (комплекси I и II) на цитохроми (комплекс III).
Цитохром С - комплекс протеин хромопротеин, чиито протезна група - хем - съдържа променлива валентност желязо (Fe 3+ в окислена форма и Fe2 + в редуцирана форма). Цитохром С е разтворим съединение вода и се намира в периферията на вътрешната митохондриална мембрана в хидрофилна фаза. Биологичната роля на цитохром с - електронен транспорт в дихателната верига от комплекса III до комплекс IV.
14.1.4. междинно съединение електронен носител в дихателната верига са разположени в съответствие с техните редокспотенциал. В тази последователност, способността да дари електрони (окисляване) намалява и способността за свързване електрони (възстановяване) увеличава. Най-голяма способност да дари електрони има NADH-голямата способност за свързване електрони - молекулен кислород.
Фигура 14.3 илюстрира конструкцията на известна част от реактивни междинни носители на електрони и протони в окислен и редуцирана форма и тяхното Взаимното превръщане.
Фигура 14.3. Взаимното превръщане на окислени и редуцирани форми на междинни носители на електрони и протони.
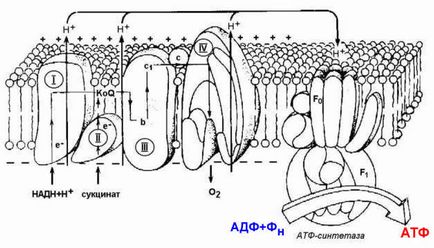
Фигура 14.4. Местоположение дихателната верига ензими и АТФ синтаза във вътрешната митохондриална мембрана.
На протоните в пространство intermembrane получени поради енергия електронен трансфер, се движат отново в митохондриалния матрикс. Този процес се извършва чрез ензима H + -зависима АТР-синтетаза (Н + -АТР-аза). Ензимът се състои от две части (виж фигура 10.4.): Водоразтворим част на катализатора (F 1) и потопени в мембрана канал хидрофилен (F) 0. Преход на Н + йони от област на по-висока към по-ниски тяхната концентрация придружава от освобождаването на свободна енергия, поради което се синтезира АТР.
14.1.6. Натрупаната под формата на АТР енергия, се използва в тялото на различни биохимични и физиологични процеси. Не забравяйте основните примери за използване на енергията на ATP:
1) Синтез на сложни химикали от опростена (реакция анаболизъм); 2) мускулни контракции (механична работа); 3) Получаване на трансмембранни biopotentials; 4) активния транспорт на вещества през биологични мембрани.
14.2.1.Stepen конюгиране на окисление и фосфорилиране в митохондриите характеризира съотношение фосфорилиране (F / G). Това е съотношението на количеството на неорганични фосфатни молекули (H 3 О 4 P) преминава в АТР към количеството на консумираните кислородни атоми (O 2).
Например, ако водородният донор на дихателната верига е молекулата на NADH. електроните от донора (NADH) на акцептор (кислород) 3 сайтове на свързване на окисление и фосфорилиране (I, III и IV ензимни комплекси на дихателната верига). По този начин, могат да се получат максимално 3 ATP молекули (ADP 3 + 3 Н 3РО 4 → 3 АТР). 1 изразходвано кислород (О2 Н + → Н 2О). коефициент на F / G = 3/1 = 3.
Ако донорът на водород е молекулата на FADH 2 в схема част дишане 2 електрони преминават конюгиране на окисление и фосфорилиране (III и IV ензимни комплекси на дихателната верига). По този начин, може да се образува максимум в 2 молекули АТР (2 ADP + 2 Н 3РО 4 → 2 АТР). Консумирана, както в предходния случай, един от кислород (О2 Н + → Н 2О). коефициент на F / G = 2/1 = 2.
14.2.2. По-сложен пример на фосфорилирането на изчисление коефициент - в окисляването на пируват до крайните продукти - е показана на Фигура 14.5. Този път настъпва дехидрогениране 4 субстрати (пируват, изоцитрат, α-кетоглутарат и малат) за образуване NADH и субстрат (сукцинат) FADH 2 за образуване понижено коензим окислява в дихателната верига и в фосфорилиране реакции произведени конюгат (4 х 3 ATP + АТР 1 х 2) = 14 ATP молекули. Още една молекула АТР (GTP) е оформен в субстрат реакция фосфорилиране на сукцинил-СоА. Следователно, пълно окисление на една молекула на пируват оформен 15 молекули АТР (14 от тях - с окислително фосфорилиране).
За да се изчисли количеството кислород консумира, е необходимо да се знае броя на дехидрогениране реакции на мястото на метаболитния път. За всеки окисление на редуцираната форма на коензим изисква един кислороден атом (см. По-горе). Ето защо, в нашия пример се консумира 5 кислородни атоми. Стойността на съотношението P / О се равнява на 14/5 = 2.8.
Фигура 14.5. Изчисляването на енергийния баланс на окислително декарбоксилиране на пируват и цикъл на Кребс.
Откачването дишане и фосфорилиране.
14.3.1. Прехвърлянето на електрони в дихателната верига не е във всички случаи възниква свързан с фосфорилирането на ADP. Държавата, в която субстрати окисление в настъпва дихателната верига, но АТР не се образува, наречен свободен (не-фосфорилиращ) окисление. Енергията, освободена по време на окислението се разсейва като топлина.
Откачването на окисление и фосфорилиране в митохондриите може да се случи в някои патологични състояния. Основните симптоми на такива условия могат да бъдат умора, треска, загуба на тегло, въпреки повишен апетит, задух и сърцебиене.
14.3.2. Дисоциацията на окисление и фосфорилиране може да бъде причинено от действието на редица материали, естествени и синтетични. Механизмът на действие на тези вещества се състои в това, че те са носители на протони през мембраната. Вещества, дисоциативна окисление и фосфорилиране, могат да бъдат разделени в protonophores и йонофори.
Protonophores са слаби органични хидрофобни киселини, които в анион форма (R-COO -) свързват протоните в пространство intermembrane, дифундират през мембраната и се разпадат в матрица за образуване на протони. Към тази група принадлежат, например, свободни мастни киселини, тироидни хормони, салицилати, дикумарол, 2,4-динитрофенол (вж. Фигура 14.6).
Фигура 14.6. Механизмът на действие на 2,4-динитрофенол.
Йонофори (ваниломицин, нигерицин, грамицидин) са в състояние да се включи в мембраната, като образува канал, през който може да се движи протоните и други моновалентни катиони - Na + или К + (фигура 14.7). В резултат на потенциалната протона се отстранява и синтезата на АТР е прекъснато.
Фигура 14.7. Ваниломицин улеснява клетъчното усвояване на Н + йони.
Свързани статии
