Вода омекване - процесът на намаляване на твърдостта на водата, т.е. намаляване на концентрацията на калциеви и магнезиеви йони.
Методи вода омекотител:
Термично омекотяване на вода
· Reagent омекотяване на вода
Термично омекотяване на вода въз основа на загряване на вода, дестилация, и зимни условия. Временната твърдост на водата, образувана от водородни карбонати на калция и магнезия се елиминира напълно под обратен хладник в продължение на един час. В процеса на варене разтворими бикарбонати превръщат в неразтворими карбонати, които попадат под формата на бяло твърдо вещество или утайки с освобождаването на въглероден диоксид в този случай. Твърдостта на водата е почти напълно отстранен чрез термична дестилация (дестилация) вода като катиони и аниони не преминават в пара.
Реактив за омекотяване на водата. Два метода на химически омекотяване на вода: вар и вар сода. Тези методи за пречистване на вода, се основават на прехвърлянето на Са2 + йони и Mg2 + йони в съединение с ограничена разтворимост на калциев карбонат СаСОз 3 и магнезиев хидроксид Mg (OH) 2.
Твърда омекотяване на вода (около 0.3 ммола / дм 3), получена чрез добавяне на вар, натриев хидроксид или сода (метод вар сода):
С гасена вар също реагира разтваря във вода, CO2 въглероден диоксид:
Тъй като омекотител се прилага като тринатриев фосфат Na3 РО4. премахване на временна и постоянна твърдост, и позволява по-пълно омекване (0.015 ммола / дм 3). Тринатриев фосфат е част от съвременните детергентни прахове.
Йонен обмен. Йонообменни и йонообменни смоли се прилагат на 60-те години. Йонообменни смоли (адсорбенти - йонни топлообменници) - твърд, неразтворим материал под формата на фини топки. В основата на тези смоли е синтетичен матрица (рамка), съдържащ положителен или отрицателен заряд и противойон компенсиране зареждане на матрицата. Чистата вода е резултат от обменните елементи (положително или отрицателно въздействие) йонообменни смоли матрични елементи на разтворените примеси. Така, концентрацията на разтворени замърсители значително намалява. Впоследствие, по време на регенерация на системи за пречистване на вода, натрупаните замърсявания от вода, изпускани във дренаж.
С малък излишък от твърдостта на водата и на сух остатък във вода, се прилага Натриев - катионобменна смола. При преминаване на твърдия водата през катионобменна смола се обменя катиони Са2 + и Mg2 + катиони Na +. са включени в състава на смолата така катиони Са2 + и Mg2 + остават на смола и Na + катиони отиват в омекотяване вода. Накрая, всички катиони Na + катиони се разменят за втвърдяване катионобменна смола губи способността му да смекчи вода и трябва да се регенерира. За тази цел, смолата се промива със солев разтвор на натриев хлорид, което води до обратния процес на омекване натриеви катиони се прехвърлят в състава от смола, като по този начин изместване катионите на калций и магнезий в промивната вода, излива се в дренажните канали (). След това, натриев богата смола да се превърне отново готова за омекотяване.
За пълна деминерализация (дейонизация) катион филтър вода след това преминава през анионобменна. Както топлообменниците на аниони се използват смоли, получени чрез взаимодействие на амини с формалдехид и полиетилен полиамини с епихлорохидрин.
Смесване зърно катионен обменник и анионния обменник на това е възможно да се произвеждат едновременно екстракция на катиони и аниони от вода.
техники за обработка на вода Мембранни - филтруване чрез специална мембрана. В зависимост от размера на порите на мембраната се разграничат микрофилтруване, ултрафилтруване и нанофилтруване. Микрофилтриране позволява да изберете размера на примес по-голяма от 0.1 микрона; се използва в медицината, хранително-вкусовата промишленост предприятия, които произвеждат алкохолни и безалкохолни напитки, за пречистване на вода в системи за пречистване на вода. Ултрафилтрация мембрани с размер на порите от 20 до 1000 А (или 0,002-0,1 mm) и се оставя глобата забавяне и колоидни примеси, макромолекули (долна граница на молекулно тегло от няколко хиляди), водорасли, едноклетъчни микроорганизми, кисти, бактерии и вируси и т.н. .d. Нанофилтриране се използва за получаване на свръхчиста вода свободни от бактерии, вируси, микроорганизми, колоидни частици от органични съединения (включително пестициди), молекулите на соли на тежки метали, нитрати, нитрити и други замърсители.
Обратната осмоза. Информационните техники монтаж и вода пречистване започва да се използва, 1960 осмоза - спонтанно преход на вещество през полупропусклива мембрана, разделяща два разтвори с различна концентрация или разтвор и чист разтворител. Като цяло разтворено вещество от разтвор с висока концентрация се опитва да се движи към разтвор с ниска концентрация. Ако налягането тласък в разтвор с ниска концентрация, поток пермеат ще спре. Диференциална поток налягане престава вещество (филтриране) през мембраната се нарича осмотичното налягане. Осмотичните явления са изключително често срещани в растителния и животинския свят. Осмоза осигурява проникване на хранителни вещества в клетката и място в извънклетъчната среда на отпадъчни продукти. метод на обратната осмоза разделяне се нарича разтвори, в които почистват вода се подава под налягане 3-8 МРа в полупропускливата мембрана, където вода се филтрира през порите и разтвореното вещество остава.
Водата, която бе пречистен чрез обратна осмоза или нанофилтрация със свойства, подобни на древните ледниците стопи вода, което е признато като най-чистите.
Определя карбонат, без карбонат и магнезиев твърдост. Въз основа на тези данни, изчисляване на размера на вар и сода, трябва да премахнете скованост.
общата твърдост на водата (общата сума на калциеви и магнезиеви йони) може да се определи от комплексометричното - титруване разтвор Трилон В в присъствието на хромогенни показатели комплексометричното индикатор - синьо или черно в амонячен среда (рН 9 - 10). Този метод се основава на факта, че калциеви и магнезиеви йони се свързват Трилон B в комплексното съединение. В този случай, следните реакции (например, Са 2+)
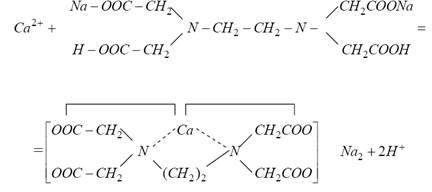
заместители на метални за водородни йони и карбоксилни групи се свързват едновременно координация връзка с азотните атоми. Независимо от заряда на катион в реакцията на комплексообразуване участва EDTA един анион и един метален катион, където има разпределение на два водородни йони. На края на реакцията се съди по промяната на цвета комплексометричното индикатор [1] eriohromovogo черен Т от вино-червен до сиво-син. Появата на сиво-син цвят показва липса на Са2 + и Mg2 + йони в разтвор, т.е. пълно свързване на Трилон Б.
