От правила Льо Шателие, то следва, че повишаването на налягането е положително въздействие върху равновесието на реакцията на окисление в - той ще се измести към образованието и да се увеличи скоростта му, за увеличаване на налягането, тук е еквивалентно на увеличаване на концентрацията и да участват в реакцията. С увеличаване на налягането, обемът на устройства в системата за контакт може да бъде значително по-малък. Въпреки това, повишено налягане в контакт сярна киселина производствения процес не е получил прилагането. Това се дължи на факта, че с увеличаване на налягането има трудности при избора на катализатора и в процеса на хардуер дизайн, докато при атмосферно налягане и може да се получи достатъчно висока степен на контактуване и скоростта на процеса поток. Освен това, при прилагане на налягане е необходимо да се компресира газът, който съдържа много азот не участва в реакция R. Д. Тя е в компресия непродуктивно консумира енергия.
3.1.3 Влияние на първоначалния състав на газовете
Теоретичната степента на окисление варира в зависимост от първоначалния състав на газове на пещта (при налягане от 1 атмосфера и температура 475 ° С), както следва:
види от данните в таблица 7, че увеличаването на концентрацията на кислород в пещта газове и свързано намаляване на процентното съдържание на окислителни увеличава.
Таблица 7 - Влияние на състава на реакционната смес
Процентът на газове на пещта
Процентът на газове на пещта
Теоретичната процентът на окисляване
3.2 катализатори за окисляване
За каталитичната активност на някои метални оксиди и платина даде представа за следните данни в таблица 8.
Таблица 8 - Влиянието на катализатори на реакцията
Максимална превръщане в%
Температурата, съответстваща на максималната превръщане на
Най-активен катализатор е платина, но отпаднал от употреба, поради високата цена и лесни otravlyaemosti стрелба газови примеси, особено арсен. Железен оксид е евтин, но конвенционален състав газ - 7% SO2 и 11% О2 то проявява каталитична активност само при температури над 625 ° С и поради това се използва само за първоначално окисляването на SO2 [4]. Ванадий катализатор по-малко активни от платина, но по-евтино и отровен от арсенови съединения е няколко хиляди пъти по-малко от платина; това е най-ефективно и само той се използва в производството на сярна киселина.
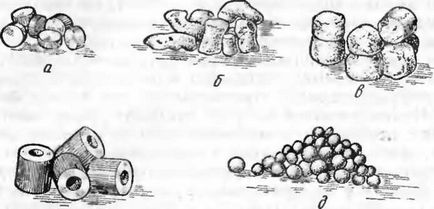
и - таблетката; Ь, - гранули; г - маса с форма на пръстен; г - на топка с форма на пелети за кипящия слой
Фигура 2 - контактни формоване Видове масови
3.2.1 Видове ванадиев катализатор
Ванадий катализатор, получен различни състави. Обикновено тя се нарича в съкратена форма първоначалните елементи на знаците, които съединенията са включени в състава му. Ние използвахме катализатори BAS (барий, алуминий, ванадий) и SVD (сулфо-ванадат инфузорна).
BAS (барий, алуминий, ванадий) състав:
поддържа катализатор активатор
SVD (сулфо-ванадат-инфузорна) състав:
поддържа катализатор активатор
За получаването на бариев катализа alyumovanadievogo-тор (BAS) се смесват при загряване до 70 ° С алкално-състезания създава ванадат KVO3 калиев силикат с разтвор на калиев К2 О · nSiO2 (течна калиев стъкло). Получената смес се прибавя бавно при непрекъснато разбъркване разтвор на солна киселина на алуминиев трихлорид AlCl3 и воден разтвор на бариев хлорид BaCl2. бяла флуоресцентна утайка се филтрува на филтър преса, след притиснат в хидранти кристал преса до съдържание на влага в 40-45%. Получената влажна маса се оформя като пелети, гранули или ко-пръстени. Overmoulded маса се изсушава до съдържание на влага в него на 15% в продължение на 30 часа, като постепенно повишаване на температурата от 60 (в началото) до 115 ° С (след сушене). Сухото тегло на ванадий контакт БАС съдържа ванадий по отношение на V2O5 7-8%. Обемната плътност на гранулиран катализатор от около 450-500 г / л.
, Получен катализатор се третира с (наситен с) серен диоксид. Този процес трябва да се извършва внимателно, тъй като то е придружено от значително отделяне на топлина и е възможно прегряване на катализатора, което води до синтероване и загуба на контакт маса своята дейност. За да се премахне контакт насищане маса прегряване са слаби серен диоксид, съдържащ не повече от 0,5% SO2. При насищане образува сулфати разпределени хлоро катализатор придобива жълтеникаво оцветяване, неговата обемна плътност се повишава до 600-650 г / л, и при което обемът се намалява до известна степен. Катализаторът се насища със серен диоксид е най-често растенията в контакт устройства.
За получаване на катализатор ванадий SVD (сулфо-ванадат диатомея) diatomit- изходни материали са инфузорна пръст, ванадиев пентоксид, калиев бисулфат и гипс. Те се смилат в топкова мелница, смесват в смесител с малко количество вода до паста и след това масата се образува в пелети или пръстени. Overmoulded катализатор се изсушава и калцинира при 500 до 700 ° С. По този начин губи вода и се превръща KHS04 калиев бисулфат калиев пиросулфат
който образува с активния комплекс. Полученият катализатор не изисква насищане на серен диоксид. Той има висока механична якост. Гранули SVD ванадиеви катализатори имат светлокафяв цвят, средната им диаметър 3.5 mm, обемно тегло от 570-600 г / л. SVD катализатор формован под формата на пръстени с външен диаметър 8-12 mm, вътрешен диаметър 2.5-4.5 мм и височина от 8-12 мм пръстени. [4]
При нагряване ванадиев катализатор над 650 ° С по време на употреба в апарат контакт неговата активност намалява относително бързо. Причините за това не е добре установена. Очевидно, когато прегряване на структурата на катализатор се променя, като намалява порьозността и активна повърхност. Освен това, когато температурата се повиши над 650 ° С може да се получи калиев взаимодействие носител силициев диоксид, при което активният комплекс се унищожава и освободен.
Свързани работи:
Концепции на съвременната наука (химическите съставки)
Учебник >> химия
реакцията се оставя да се постигне висока производителност на реактора. което е сравнимо с изпълнението на цялото. разглеждането на размера на химичните реакции се нарича химична кинетика. I. Основната идея на химична кинетика, е концепцията за скорост.
Начални стъпки на химични реакции (основно теоретичния)
и повтаряне на основните ponyatiyahimicheskoy кинетиката. Основна ponyatiyahimicheskoy кинетика Концентрация на веществото. т се заменя чрез разделяне с т (поточен реактор): (3), където Fi -. условия (реакторни gradientless поток. пълно смесване на реактора), след това.
Методи за решаване на проблеми на теоретичните основи на химическата технология
Диплома теза >> химия
промишлен мащаб. Основната концепция на химически кинетика е концепцията за скорост на реакцията, че. кРа и 293 К. обем реактор от 0,2 L, скоростта на реакцията е. Продуктът, ако изхода от реактора е известен брой ν вещества (A) = 2.
Химически науки и производство
Обобщение финансови науки >>
разходи за суровини и енергия, дизайн реактор и устойчиви на корозия материали за производство. това ниво и описание на химичния процес представи концепцията - macrokinetics с тази задача. реагент поток; ниво реактор. където описанието на феномена.
Концептуални нива в познавателната способност и химически вещества на системата (2)
състои, тъй като предполага наличието на точна ponyatiyahimicheskogo елемент. Определяне Р. Бойл като елемент. реагентите, както и влиянието на разтворителя, стените на реактора и други условия. Тя не трябва да бъде, обаче.
Свързани статии
