Фигура 24. Окислението на желязо parabolically: 1-975 0 ° С, 9-650 0 ° С
Постоянна стойност в горното уравнение може да бъде изчислена от = 0, М = M0. Тогава уравнението е:
Делът на взаимодейства форма = 1 - M / M0 параболичен уравнение може да се трансформира в:
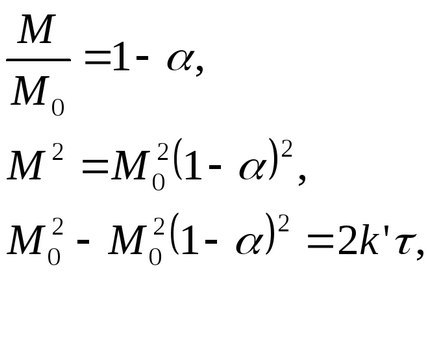
Ако твърдото вещество има сферична повърхност, цитираната по-горе решение е неприложим поради Fnepreryvno намалява по време на реакцията. Предложени са няколко решения на този проблем: някои от тях са приблизителни, точната част.
Приблизително разтвор Yandera (1927).
Скоростта на растеж на реакционен продукт е обратно пропорционална на дебелината от него:
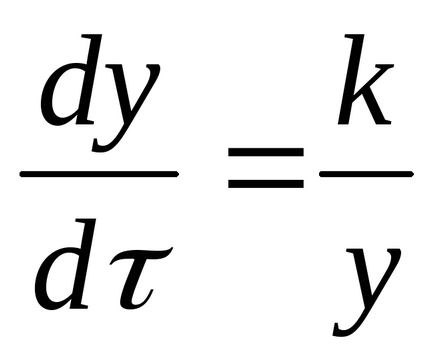
Ако r0 - начална радиус на частиците, нереагиралия дял ще
;
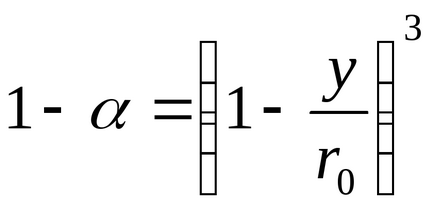
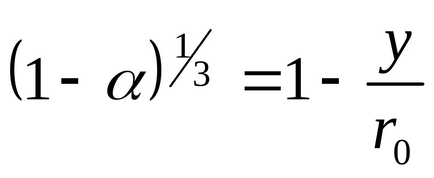
Заместването на стойността на уравнението YV (109), получаваме
Графика 1- (1-) 1/3 2 спрямо времето ще даде права линия.

