За един атом, има два основни варианта подлежат на никакво право-ЕД октет. Първият от тях - образуването на йонна връзка. (Втори - образование, на ковалентна връзка от нея ще бъдат обсъдени по-долу.). При образуването на йон-солна връзка метален атом губи електрони и става не-метален атом. Например да приемем, електронната структура на натриеви и хлорни атоми:
Na 1s 2s 2 2 2p 6 3s 1 - един електрон външно
Cl 1s 2s 2 2 2 2p 6 3s 3P 5 - седем електрони външно
Ако натриев атом предава своя един електрон Zs хлорен атом, октет правило е изпълнено за двата атома. Ще има осем хлорни атоми на електроните в картонената третия слой, като натриеви атоми - и осем електрони във втория слой, който се превръща външен:
Cl - 1s 2s 2 2 2 2p 6 3s 3P 6 - осем електрони външно
образуване йонна връзка
ядрото натриев атом все още съдържа 11 протони, но общият брой на електрони се намалява до 10. Това означава, че броят на положително заредени частици в един по-голям от броя на отрицателно зареден, следователно общата натриев заряд "атом" е едно.
"Atom" хлор сега съдържа 17 протона и 18 електрони и заряда е -1.
Заредени атоми образуват от загубата или придобиване на едно или повече електрони се наричат йони. Положително заредени йони се наричат катиони. и отрицателно заредени аниони се наричат.
Катиони и аниони, които имат противоположни заряди се привличат една към друга чрез електростатични сили. Това привличане на противоположно заредени йони се нарича йонна връзка. Той възниква в съединенията образувани от метал и една или повече неметали. Следващите съединения отговарят на тези критерии и имат йонна природа: MgCl2. Fel2, Жалби, Na2 0, Na2 S04. Zn (С2 H3 02) 2.
Има и друг начин за снимки на йонни съединения:
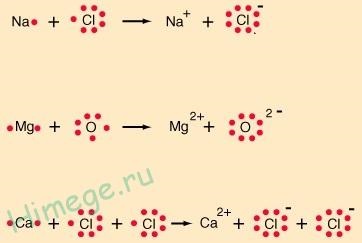
В тези формули, точки показват само електроните при външните обвивки (валентни електрони). Тези формули се наричат Lewis формули след АМЕ Рико химик G. Н. Lewis, един от основателите (заедно с L. Полинг) химическо свързване теория.
Прехвърлянето на електрони от метал атом, към атом и неметални-образование на йони възможно благодарение на факта, че неметалните елементи имат висока Електроотрицателност и метали - ниска.
Поради силното привличане на йони помежду си йонни съединения са предимно твърди и имат относително висока точка на топене.
Йонна връзка се образува чрез прехвърляне на електрони от един атом на IU талий неметални атом. Полученият йони Пр-Giwa заедно чрез електростатични сили.
Свързани статии
