Име: За проучване на емисионния спектър на атомен водород във видимата област (серия Balmer)
Тема площ: Физика
Описание: Lab № 16 ИЗСЛЕДВАНЕ емисии спектър на атомен водород във видимата формула на балмер Цел: да се определи честотата на спектралните линии във видимия спектър и емисията на водород да се изчисли стойността на константата Rydberg. оборудване:
Размер на файла: 69.5 KB
изтеглен на работа: 18 души.
Лаборатория № 16
емисии ИЗСЛЕДВАНЕ спектър на атомен водород във видимата област (Balmer серия)
Целта на работата. определи честотите на спектралните линии във видимия спектър и емисията на водород да се изчисли стойността на константата Rydberg.
Оборудване. водород лампа, неонова лампа, леща, монохроматор 2 или PA-МАМА.
Кратка теоретична информация
Излъчване на светлина се появява на порции атома # 150; лъчи при прехода на електрон на атом от един стабилно състояние в друго, повече енергия е ниска. фотонна енергия е равна ч . където з # 150; Константата на Планк,
# 150; честота на излъчваната радиация.
Според квантовата механика, честота зависи от енергията на стационарни състояния на електрони в атома, както следва:
където Е п и Е к # 150; началната и крайната енергия на стационарни състояния на атома, съответно; к # 150; броят на нивото на енергията на атома, който е направен от електрон преход след радиация, п # 150; номер ниво, от което електрон се движи, когато атом емисията на електромагнитна енергия. R # 150; Rydberg постоянен; с = 3 ∙ 10 август м / сек # 150; скоростта на светлината във вакуум.
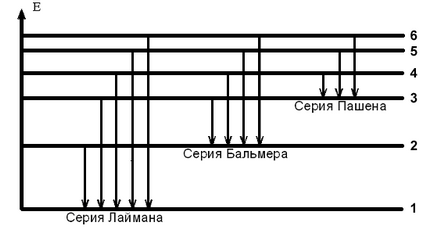
водородни спектрални линии са групирани в серия (вж. Фиг.1).
Лиман серия от линии се случва в прехода на електроните от по-висока енергия на стационарни състояния, в първата. За тези редове
к = 1, п = 2, 3, .... и честотите са в невидимия ултравиолетовата област на спектъра.
Линиите във видимата част на спектъра # 150; Балмер серия # 150; характеризиращ се с електронни преходи от страните с числата п = 3, 4, 5, ... в състояние
с номер к = 2. прехода на електрон състояние п = 3 състояние с к = 2 съответства на червената линия в спектъра, прехода от състояние на п = 4 в състояние с к = 2 # 150; зелено-синя линия и преход от състояние п = 5 в състояние с к = 2 # 150; пурпурна линия в спектъра на водород.
Преходи електрони на ниво с номер к = 3 с по-високи нива на енергия образуват серия от Paschen линии, чиито честоти са в невидимия инфрачервения диапазон и т. D. Всяка спектрална линия съответства на определена честота и дължина вълна. свързани с
В тази книга, че е необходимо да се определи експериментално честотите на трите наблюдаваните линии на серията Балмер. Използване на получените резултати, изчислени от формула (1) Rydberg постоянна.
Честотите водород спектър се измерва с помощта на монохроматор UM-2, оптични схема е показана на Фиг. 2. Светлината от водород лампа 1 се фокусира от обектив 2 върху вход процепа на монохроматор 3. Процепа е във фокуса на обектива 4 и влиза подвижната част на монохроматор, т.нар колимационния. Завъртане на копчето 5 може да се премества по протежение на оптичната ос на колиматора. Coming обектив 4 паралелно лъч светлина попада върху призмата 6 и в спектъра. Обектив 7 фокусира спектъра в областта на наблюдение. Проследяване спектър през окуляра 8. окуляра има резбован пръстен, който може да бъде постигнато чрез завъртане на острите наблюдение модел спектър. В долната част на междината 3 е винт микрометра, което позволява да се променя ширината на прореза.
снимка на спектъра се наблюдава чрез въвеждане в средата на зрителното поле на правото на неговата площ. За тази барабана 9 се завърта в дясно от монохроматор на телескопа. Барабанът е снабден с мащаб, позволяваща да се определи въртенето в градуси. Интервалът на скала е 2 . Брой на спектралните линии произведени по време на комбиниране съответствие с стрелка # 150; показалеца в центъра на зрителното поле. Arrowhead и снимка на спектъра, следва да се отбележи също толкова рязко. За да направите това, поставете окуляра остра стрела тройка часовник, след това завъртете копчето 5, постигнат остър картина на мониторинг на радиочестотния спектър. вход цепка има клапан 10, прекъсване на светлинния поток. В работно положение, че клапата трябва да бъде отворен.
барабан мащаб е оценена при честоти. За тази цел, добре проучени спектър неон емисия, описани в таблица. 1.
Описание спектър неон емисии
Забележка. За да се улесни наблюдението на червената линия 1. червено # 150; оранжево линия 2 и линия 3 всички жълто червени и жълти част на спектъра на неон е показано в отделна фигура за игра лабораторията.
Редът на изпълнение
1. Инсталирайте оптична релса радиация неонова лампа и го насочи към входния отвор на монохроматор. Задайте минималната ширина на процепа. Наблюдавайки през окуляр спектър на неон, се комбинира с показалеца на стрелката всяка от линиите, описани в таблица. 1. Ъгълът на въртене на скалата на барабана и дължината на вълната на таблицата. 1 за всяка линия, въведете
Таблица. 2. Преминаването от ярко червени, оранжеви и жълти линии до слаби линии в зелено и синьо райони на спектъра, е необходимо постепенно да се увеличи ширината на процепа.
Номер неон спектрална линия
2. Използване на таблицата с данни. 2, за изграждане на калибрационна крива на ъгъла на въртене на честотата. Когато заговор да се придържат към следната скала. На ос "честотата" на 1 см трябва да съответства ∙ 10 10 12 Hz, на "въртене ъгъл 'оста 1 см трябва да съответстват на 100 барабан въртене.
4. Запиши в бележника на маса. 3 показания барабан мащаб, съответстващ на всеки от наблюдаваните спектрални линии на водород.
5. Използване на конструираната калибрационната крива за определяне на линиите на честотния спектър на водород.
6. На фиг. Един набор числа п и к нива на началната и крайната електрон състояние за всяка линия спектър на водород. Резултатите се записват в таблицата. 3.
7. Съгласно формула (1) се изчислява Rydberg константа за всеки БАЛМЕР линии. Виж средната стойност на константата Rydberg и в сравнение с таблична стойност R = 1,097 ∙ 10 юли М-1.
Спектралният линия на водород
Drum ъгъл на завъртане (градуси)
Номер горното ниво н
Броят на по-ниско ниво
Rydberg
R (m-1)
1. Защо се приема за обхвата на калибриране на неон? Мога ли да използвам набор от други елементи на радиация?
2. Списък на серия от спектъра на водород. Кои преход съответства на главата на всеки ред от поредицата?
3. Какво определя границата на поредицата? Защо е интензивността граничния серия намалява?
4. Как преходи съответстват на линии на видимата част на спектъра на водород? Каква е спектрална серия?
до лабораторията номер 16
Както и други работни места, които да ви интересуват
Maroussia Churai Костенко Lіna ROZDІL znayshlas на I Yakbi Горящи книга Pid часа Pozhezhi Poltavі през 1658 Roku zgorіli OAO Всички документи mіskih съдове Реф. А mozhlivo Середа тях могат да б знам прав Marusі Churai. Право tsya rozglyadalasya на един от sudіv с кола vbivstva Козак.
