Определянето на молекулното тегло се извършва по различни методи. Osmometric, гел филтрация, оптични, и т.н., но най-точно е седиментационния метод, предложен от Т. Svedberg. Той се основава на факта, че чрез ултрацентрофугиране ускорение до 900000 гр процент протеин отлагане зависи от тяхното молекулно тегло.
Най-важно свойство на протеини е тяхната способност да проявяват както киселинни и основни, тоест, да действа като амфотерни електролити. Това се постига чрез различни дисоцииране групи, включени в радикали на амино киселина. Например, киселинните свойства на протеин свързан карбоксилни групи на аспарагинова киселина и глутаминова амино алкална - радикали аргинин, лизин и хистидин. По-дикарбонови аминокиселини, съдържащи се в протеина, по-изразени неговите киселинни свойства, и обратно.
Същите тези групи се имат електрически заряди, които формират общото облагане на молекулата на протеина. В протеини, контролирани аспарагинова и глутаминова аминокиселини, протеини заряд е отрицателен, излишъкът от основните аминокиселини, свързани с положителния заряд на молекулата на протеин. Вследствие на електрическото поле в протеините ще се движат към катода или анода в зависимост от стойността на общия заряд. По този начин, в алкална среда (рН 7-14) изпраща протон протеин и отрицателно заредена, докато в кисела среда (рН 1-7) се потиска от дисоциацията на киселинните групи и протеинът превръща катион.
По този начин, детерминанта на поведението на протеина като катион или анион, е реакционната среда, която се определя от концентрацията на водородните йони и се експресира от рН. Въпреки това, при определени рН брой положителни и отрицателни заряди и изравнява молекулата става електронеутрални, т.е. тя няма да се движат в електрическо поле. Тази стойност на рН се определя като изоелектричната точка на протеини. Когато този протеин е най-малко стабилно състояние и с малки промени на рН в кисела или алкална страна лесно се утаява. За по-голямата част от природен протеин изоелектричната точка е в леко кисела среда (рН 4.8-5.4), което показва, преобладаването на дикарбоксилни аминокиселини.
амфотерни свойства е основа на буферни свойства на протеини и тяхното участие в регулирането на рН на кръвта. РН на човешка кръв и характеризиращ постоянството е в рамките на 7.36 - 7.4. въпреки различни вещества киселинен или основен характер редовно от храна или произведени в метаболитни процеси - по този начин има специални механизми на регулиране на алкално-киселинното равновесие на вътрешната среда. Такива системи включват разгледани в гл. "Класификация" хемоглобин буферна система (стр.28). Промяната на рН на кръвта на повече от 0.07 предполага патологично развитие процес. Промяната на рН в киселата част се нарича ацидоза и алкална - алкалоза.
От съществено значение за организма има способността adsorbirovat протеини на повърхността си някои вещества и йони (хормони, витамини, желязо, мед), които са или слабо разтворими във вода или са токсични (билирубин, свободни мастни киселини). Протеините се транспортират от кръв към техните сайтове за по-нататъшни реакции или неутрализация.
Водни разтвори на протеини имат свои собствени характеристики. Първо, протеини имат висок афинитет към вода, т.е. те са хидрофилни. Това означава, че молекула, протеин като заредените частици привличат вода диполи, които са разположени около протеинови молекули, за да се образува водна или хидратация обвивка. Тази обвивка предпазва протеинови молекули от свързване и утаяване. Стойността зависи от хидратация черупката на структурата на протеина. Например, албумин се свързва по-лесно с водните молекули и има относително голям воден черупка, докато глобулини, фибриноген прикрепен вода е по-лошо и черупка хидрат и по-ниска. По този начин, воден стабилността на протеин разтвор се определя от два фактора: присъствието на протеиновата молекула и заряда разположени около воден черупката. Когато изтриете тези фактори протеин утаява. Този процес може да бъде обратим и необратим.
Обратимо утаяване протеин (изсолване) включва протеина да се утаява под действието на някои вещества, след отстраняване на която се връща в първоначалната си (роден) състояние. Изсолване протеини се използват за алкални и алкалоземни метали (най-често използвани в практиката на натриев сулфат и амониев). Тези соли се отстраняват чрез водна риза (причина дехидратация) и премахване на заряда. Между количество вода плик молекулите на протеин и концентрацията на сол, има пряка връзка: по-малка обвивка на хидрат, толкова по-малко е необходимо сол. Така глобулини като тежки и големи и малки молекули воден обвивка утайка от непълна разтвор насищане соли и албумини като малки молекули, заобиколени от голям вода обвивка, - при пълно насищане.
нативния протеин молекула
Денатуриран протеин молекула. Тиретата означават връзки в молекулата на спукване денатуриране на нативния протеин

eobratimoe отлагане свързан с дълбоки промени в вътрешномолекулна структура на протеина, което води до загуба на естествените си свойства (разтворимост, биологична активност и т.н.). Такъв протеин се нарича денатуриран и процеса на денатуриране. Денатуриране на протеините се извършва в стомаха, където има силна кисела среда (рН 0.5 - 1.5), и насърчава разцепване на протеини с протеолитични ензими. Денатуриране на протеини като основа за лечение на отравяния с тежки метали, когато на пациента се прилага орално ( "орално") сурово мляко или яйца, за да метали денатуриране на протеините на мляко или яйца.
Адсорбиран върху повърхността им и няма ефект върху стомашната лигавица и червата белтъци на обвивката, и не се абсорбира в кръвния поток.
Размерът на протеинови молекули е в диапазона от 1 микрон до 1 пМ, и следователно, те са колоидни частици, които са във водата за образуване на колоидните разтвори. Тези разтвори се характеризират с висок вискозитет, способността да се разпръсне видими светлинните лъчи, не преминават през полупропускливата мембрана.
Вискозитетът на разтвора зависи от концентрацията на молекулното тегло и разтвореното вещество. Колкото по-високо молекулно тегло, по-вискозен разтвор. Протеини и високомолекулни съединения молекулни образуват вискозни разтвори. Например, яйчен протеин разтвор във вода.
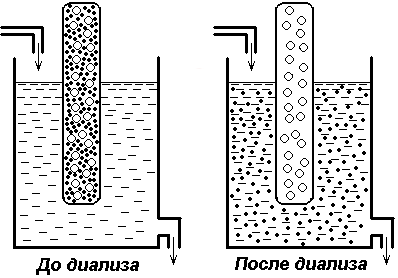
olloidnye частици не преминават през полупропускливата мембрана (целофан, колоиден филм), тъй като техните пори малки колоидни частици. Непроницаема протеин са всички биологични мембрани. Този имот протеинови разтвори обикновено се използват в медицината и химията за пречистване на протеинови препарати от примеси. Такъв процес на отделяне, наречен диализа. диализа феномен стои в основата на апарат "изкуствен бъбрек", който се използва широко в медицината за лечение на остра бъбречна недостатъчност.
Диализата (големи бели кръгове - молекула, протеин, черен - молекула на натриев хлорид)
Мляко минерали
Структурни и механични свойства на маслото.
Според Rebinder има два основни вида структури.
Първият тип - коагулация структура - пространствена решетка, произтичащи от безразборно адхезия на минута частици от диспергираната фаза или тънки rassloyki макромолекули през средата.
Вторият тип - структура на кристализация кондензация. образуван чрез директно сливане на кристали при което се образува поликристален твърдо вещество.
Дебел базирани маргарин са тип коагулация структури. Последователност и пластмасови свойства на маргарин мастни основи се определят главно от съотношението на твърди и течни фази в определена храна мазнини. Тази връзка разделяне характеристика твърдо вещество-течност на някои специфични условия за кристализация (температура, време, възбуда). В тази важна част от непрекъсната среда и дисперсна фаза и Разпръснатите фазовия характер в непрекъснат течна среда.
За някои видове на годни за консумация мазнини при определени температурни условия и кристализация количество твърд диспергирана фаза може да излиза извън границите на оптималното фаза връзката и след това върху повърхността на кристалите образувани като непрекъснат слой на течната среда, те не могат да наруши хаотично масата на кристали снадени един с друг. В този случай, ние винаги ще има най-високата твърдост на мазнините база kroshlivuyu последователност и най-лошите пластмасови свойства.
Ако стайна температура течност непрекъснато среда са оптимални дебелина на слоя, т.е. тези, които не се създадат условия за снаждане на кристали по време на съхранение, по време на механични или термични въздействие върху системата, в този идеален случай, ние винаги ще се втвърди коагулация структура, които определят свойствата на най-добрия пластмасата на базата на мазнини.
За получаване на коагулацията усилени структури като най-добрите пластмасови свойства, в чужбина често се въвеждат в мазнини база формулировка са два вида хидрогенирана мазнина с температура на топене 32 ° С и 42 ° С Когато това се въвежда значително количество течни растителни масла. Над, от една страна, той създава най-доброто съотношение на мазнини, базирани на твърди и течни фази, за да се осигури съгласуваност, сходен с маслото, и от друга страна, създава условия за постоянството на консистенцията на маргарин в доста голям диапазон от температури. Заедно с това, въвеждането на високо топене на мазнини базисни salomas е в противоречие с изискванията на физиолозите в състава на мазнините в храната.
На първо място, следва да се отбележи, че само присъствието на емулгатори високо-производителни, стабилизатори са допринесли за създаването на съвременни технологии в производството на маргарин и да се гарантира производството на хранителни мазнини с високо качество на продукта. Повърхностно активни добавки осигуряват фино разделен емулсия в силна връзка на дисперсната фаза с непрекъсната среда (твърда мазнина при стайна температура). Основният проблем при производството на маргарин - е ефектът на повърхностно активни добавки за структурните и механичните свойства на маргарин, и по-специално способността за разтваряне.
Адсорбционното слой на емулгатора повишава стабилността на емулсията, по-специално в случаите, когато този слой е по образец, образуващ повърхността на филма гел значително повишена якост и здравина.
Тези свойства са от особено значение за производство на маргарин като крайният продукт е емулсия от малки частици от течната фаза, равномерно разпределени в непрекъсната среда на твърдата фаза при стайна температура.
Проблемът на сила емулсия е тясно свързан с въпроса за типа произведен с емулсии емулгатор. Има възможност за формирането на два вида. Стойността на обемното съотношение на фазите за определен вид на емулсия, образувана поради срастване и пакет тип емулсия се появява по-интензивно, отколкото по-малък обем от средата за дисперсия и повече - диспергирана фаза. Ако емулгатор осигурява стабилна емулсия на само един вид, обемното съотношение престава да бъде от решаващо значение при определяне на вида на емулсия. Инверсия зависи не само от съотношението на обемите на фаза, но също така и от концентрацията и химическата природа на емулгатора на.
Емулгатори трябва да имат следните качества:
- за намаляване на повърхностното напрежение;
- достатъчно бързо, за да се адсорбира в интерфейса, предотвратяване на слепването на капчиците;
- да имат специфична молекулна структура с полярни и неполярни групи;
- да влияе на вискозитета на емулсията.
Ефективността на емулгатор е специфично свойство, в зависимост от природата, вида на емулгиращи вещества, температура, рН, концентрация, време, емулгиране и т.н.
Ефективността на действие, както и естеството на емулгатора определя вида на емулсия.
Хидрофилни емулгатори, по-добре разтворими във вода, отколкото в въглеводороди, допринасят за образуването на емулсии масло - вода и хидрофобен, по-добре разтворими във въглеводороди - водни емулсии - масло. Съотношението на размера на полярни и неполярни части емулгатор молекули се характеризира със специален индекс - HLB. Ако HLB на емулгатор е 3-6, емулсия вода форми - масло, със стойност на HLB на 8-13, за предпочитане образува емулсия масло - вода.
Маргарин е преохлажда емулсия на вода в масло. Това не изключва възможността за образуване на емулсия с преобладаване на смесен тип емулсия вода - масло.
Основните функции на емулгаторите:
- създаване на стабилна емулсия от фино;
- стабилизиране и предотвратяване на отделянето на влага и мазнини в крайния продукт;
- осигуряване на стабилност по време на съхранение;
- осигуряване на antirazbryzgivayuschey капацитет за пържене;
- предоставяне на пластичност;
- осигуряване на устойчива форма на кристална решетка в процеса на образуване на структура;
- осигуряване на определени функционални свойства на крайния продукт в зависимост от използването на маргарин.
В Украйна, в продължение на много години ние сме били използвани емулгатори, произведени в Русия, както и собствената си продукция, произведена на полуфабрикати. Те включват емулгатори:
- Т-1 - glycerolysis продукт от лой или хидрогенирани мазнини;
- Т2 - полимеризация продукт на глицерол естерифицирана със стеаринова киселина;
- T F - емулгатор смес T-1 и храна фосфатид концентрат в съотношение 2: 1;
- PMD - хранителни моно-диглицериди;
- ТВЕ - комбиниран емулгатор - MIT смес и фосфатид концентрат в съотношение 3: 1.
Широка гама от емулгатори Нижни Новгород растение - различни видове дестилирани моноглицериди. В момента, Нижни Новгород усвоили производството на серия от нови емулгатори, основани на лецитин. Този стандарт лецитин, фракционирано лецитин - fosfaditilholin и fosfaditilserin и хидролизиран лецитин.
През последните години в Украйна се използват главно емулгатори от различни модификации Dimodan серия, Palsgaard (някои предприятия Quest).
В различни периоди от предимство в търсенето на тези два вида емулгатори, предавани от един на друг. Можем да кажем, че тук има качеството на конкурса - цената.
В зависимост от съдържанието на мазнини маргарин и неговите емулгатори обхват употреба Dimodan PVP (Dimodan HP), Dimodan OT (Dimodan S-T PEL / B), Dimodan superlattice. За съдържание на маргарин мазнини под 40%, което в момента е в търсенето на населението се използват допълнително (с изключение Dimodan RT или Dimodan CP или Dimodan LS.) Полиглицеролови естери и рицинова киселина - ГРАЙНСТЕД PGPR90.
Трябва да се отбележи, че фирмите, които произвеждат дават препоръки за употребата на различни видове емулгатори и системите за стабилизиране, в зависимост от целта на маргарин. Спазването на тези препоръки, ви позволява да получите висококачествени продукти
Свързани статии
