Източникът на електричество в дома си.
Газ батерия с ръцете си
Във всеки батерия има положителни и отрицателни плочи с активно вещество, съставен от различни метали. Както проводимата среда обикновено се използват водни разтвори на киселини или основи. Този разтвор се нарича електролита. Когато потопен в електролит плочи ще започне химична реакция се случи, и ако те са по-близо от измервателното устройство, ние откриваме, че електрическият ток тече през външната верига.
По време на работа на батерията, както и неговото заплащане може да се види, че газовите мехури се разпределят на плочите. Газове обикновено не участват в реакции и електрохимически процеси работят в поддържаща роля, така че конвенционален батерия потенциална разлика се определя само чрез свойствата на метали от които плаката. Но се оказва, различни газове също имат добре дефинирана електрохимична потенциал. Следователно, тази възможност може да се използва за производство на батерията, в която ролята на активното вещество ще отговарят две различни газ. Газ батерия е изобретен през 1955 г. от Съветския инженер А. Presnyakov.
Важно предимство на батерията газ - простота на устройството и висока ефективност. За производството му не се нуждае от цветни метали и скъпи материали. Работна качество газ батерия също е много висока. Газ батерия може да се съхранява дълго време, при или неактивният, и това не оказва влияние върху представянето му. Той позволява на голям ток на зареждане, което намалява времето за зареждане. Дори продължителни затварящите плочи между газ безвредни за батерията, тъй като в този случай въпреки че се освобождава, но без необратими процеси в активния материал, както и в други типове батерии.
Газови батерии - структурно нови източници на електричество. създаването им е станало възможно само след вещества са открити в състояние да абсорбира газове в големи количества и задържане на доверието им. Тези вещества се наричат адсорбенти. Един от най-добрите адсорбенти - активен въглен. Усвояването газове, той не участва в химични реакции.
Таблица поставен долу показва редица различни газове може да се абсорбира от един грам от активен въглен при 15 ° С при нормално налягане. Веднага ще забележите модела: газът се абсорбира по-добре от по-горе своя критична температура, което означава, че по-лесно се втечнява.
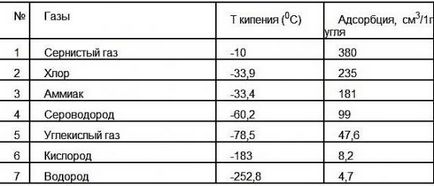
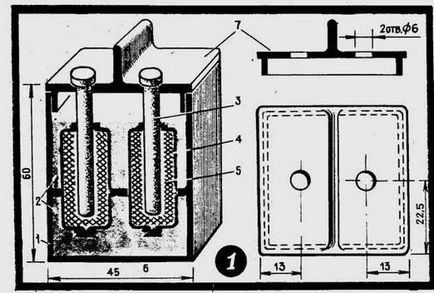
Структура самоделно газ акумулатор е показано на фигурата. Контейнерът 1 се излива електролит 2. електролитни пропуска двата електрода, които се състоят от сърцевина 3 и торбата 4 с активиран въглен торбички 5. Защита срещу изместване преграда 6, която е направена от всеки електрически изолационен материал. Капацитет затваря капака 7.
Батерия с ръцете си
Както капацитета на газ акумулатор може да бъде успешно използван, например, буркани подправка - те се продават в магазин за железария. Можете да вземете и стъклени буркани, но те трябва да се покрие от външната страна на асфалтов лак, така че светлината не прониква вътре, и това ще допринесе за батерията.
Измислям чанти от стари найлонови отглеждане здраво сплотена. Шевът може да бъде омрежен найлонов конец или запояване на кръгли дървени слитък.
Единият край на торбата плътно изравнителен найлонова нишка, и втора, отворена, поставете въглероден прът на батерии, фенер, излишък. Напълнете торби с активен въглен, и го уплътнява. Огъване на края на торбата, изравнителен им найлонова нишка около пръта. Сега трябва да се остри завои вратовръзка торби. Колкото повече намотки се прави, по-добре контакта на въглероден прах с пръчка, по-малката вътрешното съпротивление на батерията, толкова по-добре работи. Електродите трябва да се укрепи на корицата и на изправени пред края на прът навън да прикачите терминали.
Най-добре е да се използва медицински въглен, който се продава в аптеките, или въглища газови маски умъртвени. В краен случай, въглена може лесно да се подготвите. За да направите това, да отнеме 5-10 пръти мм диаметър, дълги (от всякакъв вид дърво) 100 мм, като ги свърже в нишка лъч, поставете кутията може и да попълните сух речен пясък. Поставете буркана във фурната върху горещи въглени или на газов котлон и запали, докато вече не се открояват от каната газове. Оставете да изстине пясък, а след това извадете овъглени парчета - те след това може да се консумира в случая. За контейнера на батерията 1 в ампер-часа изисква 50-90 грама активен въглен.
За електролита е по-добре да се дестилирана вода, които могат да бъдат закупени в аптека или в крайни случаи, кладенци, или батерия, преди и вряща вода за половин час и се охлажда. Всяка чаша вода vsypte 1-1.5 супена лъжица сол. Напълнете съда за електролит и покриване на електродите, като се уверите, че електродите са напълно потопени в електролита.
Най-простият газ батерията е готова, и сега остава само да се зарежда. За това е необходимо да се приложи на електродите към източник на напрежение DC 4.5. Поставете етикет ярка боя положителен електрод, което води до етикета на корицата. + Отрицателният електрод не могат да се поставят етикети. При повторното зареждане на полярността на стик електроди. Завършете зареждане, когато напрежението на електродите на акумулатора е 2,2-2,5 инча
При постоянна батерия на електролита трябва да се промени най-малко веднъж седмично. (Забележете, че такъв честа смяна е необходимо само за електролита, съставена въз основа на готварска сол).
С отделението за батерията. Когато зареждането, когато напрежението свързан към електродите, електролитът се разлага на водород и хлор. Електродът е свързан към отрицателния проводник ще абсорбира водород и към положителния - хлоро. По този начин, потенциална разлика.
Както електролита в акумулаторите на газ могат да бъдат използвани различни разтвори на соли, киселини и основи. С избирането на електролит, то е възможно да се извърши електролиза на тези или други газове, и да получите различен електродвижещо напрежение и капацитет на батерията. По този начин, ние се получи двойка от водород в електролизата на слаб разтвор на сярна киселина - кислород. Разтвор на сода воля двойка водород - въглероден диоксид. Като цяло избор електролит отваря широко възможности за експеримента.
Свързани статии
