- 10-те най-влиятелни Психолози
- Как да прекарват време с децата? Тук имате 100 идеи!
- Id, Его и Суперего
- Учените са критикували Маслоу пирамида
- Струп ефект: как да създадете свой собствен експеримент?
- 10 неща, които трябва да знаете за психологията
Разделение> .uk панел ">" данни-UK-решетка-марж>
Аминокиселините
Малко по химия за аминокиселини (може би някой не знае), които са едно и всички на нашите организми с вас. От биология Разбира се, все още се знае, че аминокиселините са мономери, т.е.. Е са в следствие на полимеризация за образуване на полимери от са протеини. Разбира се всички аминокиселини са органична структура.
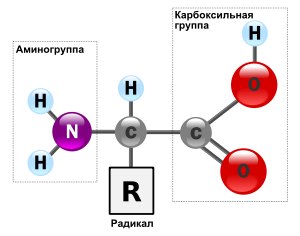
По отношение на структурата на аминокиселини, всяка аминокиселина се състои от карбоксилна (-СООН) и амино (-NH2) групи, които са свързани с един въглероден атом. По този въглерод-свързан странична верига - радикал, който е само същите свойства на детерминантите на аминокиселина.
Повечето от aminok има само една амино и карбоксилни групи, такива аминокиселини са наречени "неутрални". Въпреки това, аминокиселини съществуват повече от една амино контрабандни карбоксилна група, те се наричат "сърцевина".
Науката знае около 200 аминокиселини, които могат да възникнат в организми, обаче, само 20 от тях са част от протеина. Тези 20 аминокиселини се наричат belokobrazuyuschie или протеиногенни аминокиселини.
В зависимост от радикал, който е писано по-горе, остатък базична амино киселина е разделена на три групи:
1) неполярен (аланин, метионин, валин, про-линг, левцин, изолевцин, триптофан, фенилаланин)
2) незаредени полярни (аспарагин, глутамин, серин, глицин, тирозин, треонин, цистеин)
3) полярен зареден (аргинин, хистидин, лизин - положително; аспарагинова и глутаминова киселина - отрицателен).
За доста химици:
Странични вериги от аминокиселини (радикал) може да бъде хидрофобен или хидрофилен, което дава съответните свойства на протеини, които се проявяват при формирането на вторична, третична и четвъртична структура протеин.
В разтвор, аминокиселината може да служи като киселини, така и основи, т. Е. Те са амфотерни съединения. -СООН Карбоксилната група може да дарява протон, функционира като киселина и амин - NH2 - приеме протон, по този начин, показващ база свойства.
Забележки: Снимката показва обща формула аминокиселина.
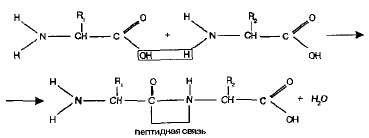
В продължение на един курс за аминокиселина искам да добавя нещо за пептидите. Сега те са широко продавани и използвани в спорта, козметика, операцията и така нататък ... Но ние ще говорим за химия, а по-скоро по органична химия, защото пептиди са органична структура. И така, това, което е peptidy- органични вещества образуват, когато амино групата на една амино киселина е способен да реагира с карбоксилната група на друга амино киселина. (За групи, виж предишната ми статия). Молекулата формира след това се нарича дипептид, и -CO-NH- връзка се нарича пептидна връзка.
От получената дипептид от една страна е свободна амино група и другата карбоксил. Поради това, дипептид е да поеме други аминокиселини, и след това образуване на олигопептид, ако по този начин се присъединява към повече от 10 аминокиселини, е оформен polepeptid. Надявам се, че е ясно)
Много хормони (инсулин, адренокортикотропен хормон, и т.н.), антибиотици (например, грамицидин А), токсини (например, дифтерия токсин) са полипептиди.
Протеините са полипептиди, които включват молекула от петдесет хиляди до няколко аминокиселини с относително молекулно тегло повече от 10 000.
Ето една много кратка малка статия, надявам се всички, научих нещо ново или повтарящи се обхванат, благодаря ви за вниманието.
