Ванадиев оксид. Характеристики naib. важни ванадий оксиди, представени в таблицата. С увеличаване на степента на окисление на амплифицираните V-киселинната свързваща WA оксиди. както и техните химически. резистентност. За много оксиди на ванадий характеризира с относително широки области на хомогенност (вж. Таблица. И фиг.).
Оксид VO не Сол. във вода; с разредена. неорганични соли. до трето образува бледо синьо или виолетово р-RY V (II) соли. Силна редуциращ агент. V2 О5 се получава чрез редукция с водород при 1700 ° С Хидроксид V (ОН) 2. образуван от действието на алкален на р-р на V (II) соли не се получава в чист вид.
Sesquioxide V2 О3 съществува в две кристални. модификации; при - 105 ° Sforma преобразува. а (преход 1.8 кДж / мол) Формата - antiferromagnet. температура Neel 168 К. водата не е зол. с неорганични соли. за да се образува сол-трет V (III). Силна редуциращ агент. V2 О5 се получава чрез редукция на въглероден окис. H2. S и др. При нагряване. Използва се за производство на ванадий бронз. като материал за термистор. Той се среща в природата като минералната karelianita. Хидроксид V (ОН) 3, образуван от действието на основи или NH4 ОН в солеви разтвори V (III), без достъп на въздух.
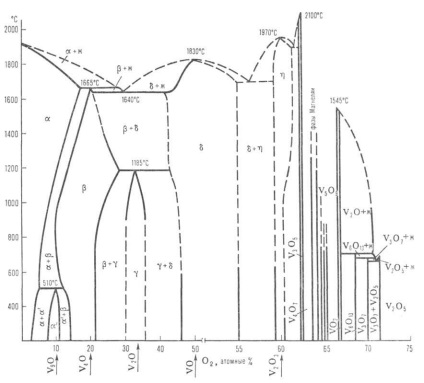
Система членка Диаграма ванадий-кислород: F-стопи; р-твърдо RY (-O2 до V; -базирани V9 О; -базирани V4 О; -базирани V2 О; базирани VO; базирани V2 Оз); прекъснати линии, показващи приблизителните граници на фазите.
Пентаоксид trivanadiya V3 О5 - antiferromagnetic. температура Neel 270 К; при 430 К придобива метален блок. проводимост.
съществува VO2 диоксид в две кристални. модификации; при 68 ° Sforma преобразува. а (преход 3.1 кДж / мол) Формата - antiferromagnet. температура Нийл К. 345 Не сол. във водата. Хигроскопична. Amfoteren: при киселинни форми р-ма ванадил VO 2+ катион (RR става светло синьо), в което алкална ванадат (IV) - сол не се изолира в Своб. izopolivanadievoy състояние (IV), за да ви-H2 V4 O9. Редуктор. Окислява на въздуха. V2 О5 се получава чрез сливане с оксалова към едно без достъп чрез нагряване на смес от въздух V2 О3 да V2 О5. окисление на V2 О3. Използва се в производството на-съм ванадий бронз. като полупроводников материал за термистор, ключове, запаметяващи елементи, и други дисплеи.
Оксихидроксид VO (ОН) 2 - розови кристали; утаява от р-ров при рН> 4. Amfoteren.
Divanadiya пентоксид V2 О5 над 700 ° С дисоциира. Диамагнитно. N-тип полупроводник; Bandgap
2,5 EV. P-rimost във вода 0.35 гр / л при 25 ° С; във воден р-ма съществува като izopolivanadievoy (V), за да-ви вероятно състав Н2 [O (V2 О5) 2,5]. B киселина р-ма вероятно - наличие форма V на (V) - VO2 + йони и VO 3+. При загряване. р-ров (рН 1-2), разпределени хидрати променлив състав V2 О5 * xH2 О. ванадати (V) са оформени в р-ма алкални. На техническата производство-съм V2 О5 см. Ванадий. Pure V2 О5 се получава NH4 VO3 разлагане при 400-500 ° С, последвано. забавяне в потока O2. хидролиза VOC13. Пентаоксид - межд. продукт в производството-положителни ferrovanadium, ванадий. ванадати и сътр. Comm. V; катализатор при получаването на H 2SO 4; специален компонент. чаши, глазури и червени фосфорни светят. Той се среща в природата като минералната scherbinaita.
* Т. бали. - 3000 ° С (разл.). ** T. бали.
Има пет ванадиеви оксиди. формиране на хомология. номер Vn O2n-1 (Magnelli фази), където U = 4-8. Представлява черни кристали с триклинен решетка. Имат метален блок. проводимост при ниска т-ма (с изключение V7 Ø13). Antiferromagnets. М. б. използван като полупроводникови материали за термистори. Ванадий също образува оксиди V3 О7 и V6 Ø13 - черни кристали моноклинни решетка топят incongruently: първо - при 660-680 ° С с образуване на V6 Ø13. вторият - при 700-710 ° С за да се образува VO2. Ванадиева оксиди са токсични. За V2 О5 MPC 0.1 мг / м 3 (дим), 0.5 мг / м 3 (прах).
===
App. Литература за статията "ванадий оксид". Pletnev RN Gubanov VA Fotiev AA NMR ванадиев оксид съединения. М. 1979 Vanadiumoxide: Darstellung, Eigenschaften, Anwendung, 1983. V. Ya Ya Slotvinsky-Сидак.
Свързани статии
