Redox реакции - реакции, проявяващи се с промяната в степента на окисление на елементите.
Окисляване - процесът на откатни електрони атом
Възстановяване - електронен процес атом Hour
Намаляване на агент - електрон на елемент даряването
Окислителят - елемент, който приема електрони
За визуално, но опростено представяне на причините за промените в елементите на обвиненията Вижте илюстрацията:
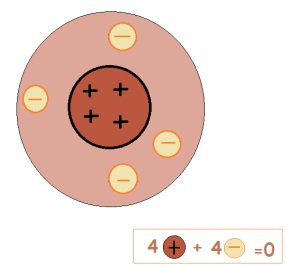
Един атом е електрически неутрални частици. Поради това броят на протоните е равен на броя на електроните
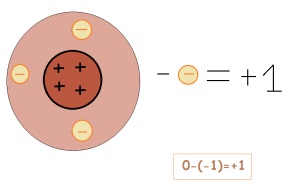
Ако даден елемент дава на електрона, заряда се променя. Това става положително заредена (ако е положително, а напротив, отрицателно)
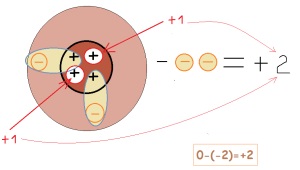
по този начин на елемент такса влияе върху броя на електроните приемат или да се хвърли
I. писане уравнения окислително-редукционни реакции vosstavnovitelnyh
1. Напишете схемата за реакция
Na + Cl2 -> NaCl
2. Ние организираме степента на окисление на елементите:
Na 0 0 + Cl2 -> Na + Cl -
3. Пишем елементи променят степента на окисление и да определят броя на гласове / получени електрони:
4. Намерете най-малкото общо кратно на броя на свързаното гласове и електрони:
