Метални връзка - вида на атомите в кристална вещества с метални свойства (метали, металоиди). Т.т. поради високата концентрация на такива кристали квази-свободни електрони (електронна проводимост). Отрицателно заредените електрони газ "свързва" положително зареден и IO ни един с друг.
Ковалентна връзка - тип химична връзка между два атома, който се извършва на тяхната обща електронна двойка (по един от всяка електрон атом). К. с. Той съществува и в двете молекули (във всички състояния на агрегация), и между атоми, съставляващи кристалната решетка. К. с. може да се свърже еднакви атоми (в Н2 молекули. Cl2. в диамантени кристали) или различни (във водни молекули в кристалите на силициев карбид SiC). Почти всички типове фиксирани връзки в молекулите на органични съединения са ковалентно (С - С, С - Н, -. N и др). К. с. много издръжлив. Това обяснява ниска реактивност на парафинови въглеводороди. Много неорганични съединения, които имат атомна кристална решетка, която се образува чрез К. р. Те са огнеупорни и имат висока твърдост и износоустойчивост. Те включват някои карбиди, силициди, бориди, нитриди (по-специално, известен borazon BN), са намерили приложение в новата техника.
Йонна връзка - electrovalent връзка, бифункционален връзка, един вид химическа връзка, която се основава на електростатично взаимодействие между противоположно натоварени йони. Такива връзки в относително чиста форма на алкални халогениди, например KF, тъй като металните атоми алкални са един слаби ограничи електрони (свързващи енергия от около 3.5 ЕГ) и халогенни атоми имат висок афинитет за електрона. Но дори и в кристали (на повече молекули) на тези съединения пълен трансфер на електрон от халогенен атом, метален атом, за по-голямата част все още се среща. Общи първите идеи за образованието в други случаи, две, три или четири пъти, йоните на Са2 +. С 2-. В 3+. Si не 4+ потвърдена, тъй като се образува химична връзка, в такива случаи по-сложен начин. За да се оцени степента на ionicity на връзката използва концепцията за ефективен заряд на йона.
Първоначалната структурата на високо въглеродна инструментална стомана U11 преди нагряване за охлаждане - перлит + карбиди.
Критичните точки за стомана U11: С = 1 730 ° С А см = 810ºS.
оптималните условия отоплението на втвърдяване за хиперевтектоидния стомана (С%> 0.8%) прави AS 1 + (30 ÷ 50 °), т.е. за U11 - 760- 780ºS. В този случай, след закаляване имаме глоба зърно, като предоставя най-добрите механични свойства на стоманата U11.
Топлина и излагане стомана U11 при 850 ° C, преди закаляване предизвиква растеж на зърно и влошаване на механичните свойства на стоманата след топлинна обработка. Груба структура води до повишена чупливост на стоманата. Понякога това води до фрактури.
Темпериращи про-евтектоиден стомана се състои в загряване на стоманата до температура над критичната он (AC3) в екстракта, и последващо охлаждане при скорост над критичната.
Температурата на точката AC3 за стоманата 30 е 820 ° С
Термична обработка, необходимо за получаване на твърдост 350 НВ, изотермично закаляване е troostite. Като охлаждаща среда за изотермични втвърдяване най-често използваната температура стопена сол, която се определя експериментално.
При температура над стомана U8 постъпления A 1 перлит на аустенит. Като резултат от охлаждането на аустенит в стопени соли, образувани от ферит-цементит структура - troostite.
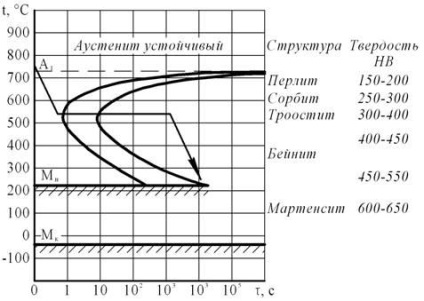
Фигура 6 - Фигура Ia изотермични превръща AY stenita стомана U8
В резултат на топлинна обработка, получен стомана твърдост 350 НВ, структура - troostite.
Основно система сплав на желязо въглероден кристализацията започва при достигане температури, съответстващи линия ABCD (ликвидус линия), и завършва при температури AHJECF образуваща линия (солид линия).
При температури, съответстващи на линия BC, течният разтвор е кристализирана аустенит. В сплави, съдържащи от 4.3% до 6.67% въглерод, при температури, съответстващи на компактдиска линия. Кристали започват да се изправи първичен цементит. Цементит, кристализиране от течната фаза, наречена основно. От точка Б при температура от 1147 ° С, а концентрацията на въглерод в суспензия 4.3% от евтектична се образува, който се нарича ledeburite. Евтектична да образуват ledeburite формула могат да бъдат написани ZHR4,3 А [A2,14 TS6,67 +]. Процесът на първичен кристализация на желязо ECF линия завършва образуват ledeburite.
Така, чугун структура под 1147 ° С ще бъде: hypoeutectic - Ledebur + аустенит, евтектична - Ledebur и хиперевтектични - цементит (първична) + Ledebur.
Transformations, срещащи се в твърдо състояние, се наричат вторично кристализация. Те са свързани с прехода когато охлажда γ-желязо в α-желязо и разлагане на аустенит.
GS линия съответства на температури, започващи трансформация на аустенит на ферит. Под линията GS сплави, състоящи се от ферит и аустенит.
Линия Е S показва начало температурата на утаяване на цементит на аустенит се дължи на намаляване на въглерод в аустенит разтворимост с намаляване на температурата. Цимент, освободен от аустенит, наречен вторичен цементит.
В точка S при температура от 727 ° С и концентрацията на въглерод в аустенит 0.8% евтектоиден смес се формира, състояща се от ферит и цементит, който се нарича перлит. Перлит се получава чрез едновременно утаяване на аустенитни феритни и цементит частици. Процесът на преобразуване на аустенит да перлит могат да бъдат написани A0,8 формула II [F0,03 TS6,67 +].
линия PQ В показва намаляване на разтворимостта на въглерод в феритни по време на охлаждане и изолиране на цементит, който се нарича третичен цементит.
Следователно, сплави, съдържащи по-малко от 0.008% въглерод (Q точка) са еднофазен ферит и имат мрежеста структура и сплави, съдържащи въглерод от 0.008 до 0.03% - структура на ферит + цементит третичен и нарича технически желязо.
Hypoeutectoid стомана при температура под 727ºS има структурата на ферит + перлит и хиперевтектоидни класове - перлит + цементит като вторично меша по границите на зърното.
hypoeutectic чугуни на 1147-727ºS в температурния диапазон от аустенит време на охлаждането се разпределят вторичен цементит поради намаляване на разтворимостта на въглерод (ES линия). При достигане на температура 727ºS (линия PSK) аустенит, въглеродът обеднен до 0.8% (точка А), трансформира в перлит. По този начин, след окончателното охлаждане структура hypoeutectic чугун се състои от перлит и цементит вторичен ledeburite превръща (перлит + цементит).
Структура евтектична чугун при температура под 727ºS състои от ledeburite преобразува. Хиперевтектични чугун при температури под 727ºS състои от ledeburite превръща и първичен цементит.
Фаза правило установява връзка между броя на степените на свобода, броя на компонентите, както и броя на фазите и се изразява с уравнението:
С = К + 1 - F,
където С - броят на степените на свобода на системата;
K - брой компоненти, изграждащи системата;
1 - броят на външни фактори (външен фактор разглежда само температурата, тъй като налягането, освен при много висока малък ефект върху равновесие фаза на сплави в твърди и течни членки);
F - брой фази в равновесие.
сплав от желязо с въглерод, съдържащ 0.01% С, наречен про-евтектоиден стомана. Неговата структура при стайна температура - ферит + цементит (първична).
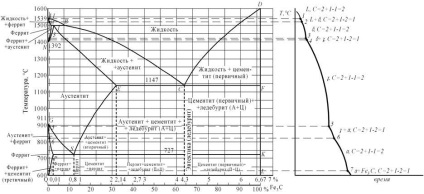
Фигура 5 диаграма на желязо-цементит,
б охлаждане крива за сплавта, съдържащ 0.01% въглероден
Свързани статии
