Моновалентни йони като натрий, наистина Con-zyvayuetsya с кисели фосфолипиди, но с нисък афинитет.
Вярно афинитет на Са2 + към повърхността на амфотерни фосфолипидни везикули близо или малко по-малки от повърхността на кисели фосфолипиди. По-силно свързване на Са2 + с кисели фосфолипиди, причинени не bblshim афинитет към него Са2 +. и електростатичен ефект е вероятно по-висока плътност на отрицателни заряди, което води до увеличаване на локална концентрация на Са2 + на повърхността.
Свързването на двете единични и двувалентни катиони, очевидно има малък ефект върху конформацията на полярни глави на фосфолипиди, поне фосфатидилхолин и фосфатидил глицерола. При свързване на фосфатидилсерин наблюдава обездвижване на карбоксилни групи.
Обикновено, Са2 + се свързва с фосфолипиди в стехиометрия на 1: 1, въпреки че в случай на фосфатидилхолин един Са2 + йон се свързва с две молекули на липид. Очевидно е, че комплексът, образуван и стехиометрията 1: 2, в резултат на метал свързване възниква агрегация мембрани; където двувалентният катион може да служи като мост между два плътно притиснати повърхности на мембраната.
Свързването на Са2 + може да доведе до промяна в състоянието на липид. Например, свързването на Са2 + с фосфатидилсерин или фосфатидинова киселина може да бъде придружено от фазов преход на двуслойна гел и взаимодействието с ct-diolipinom стабилизиран хексагонална фаза. Ако везикулите се състоят от смес от кисели и цвитерйонни липиди, свързването на Са2 + причинява странично разделяне на фазите; по този начин може да се образува обширни области в еднослойни везикули.
Предимствата му дава свързващи фосфолипиди Mn 2+. защото парамагнитни йони променя варират 31 P-NMR. Тези промени зависят от локалната концентрация на Mn2 +, и следователно могат да бъдат използвани за измерване на потенциала на повърхността.
С киселинни бислоеве повърхностно здраво свързани като поликатиони, например поли- или гентамицин.
Zeta потенциал и електрокинеза явления
Ако заредени мехурчета, се поставят в електрическо поле, те ще се движат към електрода, такса, която е противоположна на знак, за сметка на мехурчето. Електрофоретичната подвижност-LIC везикули определят т.нар зета poteitsialom което е равно на електрическия потенциал между обема на разтвора и така наречената Хелмхолц равнината, успоредна на равнината на мембраната. Тази равнина разделя дебелина част на двойно електрически слой, който се движи в електрическо поле, заедно с мембрана и се съхранява при около 2 на зарежда везикули повърхност. По този начин, степента на зета потенциала е по-малка от стойността на потенциала на повърхността и потенциала на повърхността е свързано със съотношението определя от теория Gouy - Chapman. Измерване на зета потенциала лежи в основата на един от стандартните методи за оценка на потенциала на повърхност и може да се използва за изследване на свързване на йони с veznkul повърхността фосфолипид. В електрофоретичната подвижност също се влияе от присъствието изпъкнал над повърхността на заредения двуслойна Neelie Пидна-мембранни компоненти, такива като протеини или gangliozi-редове и използване електрокинетични техники може да се получи информация за разпределението на таксите в близост до повърхността на везикулите.
Хидрофобно свързване на йони и мембранни проби
Наличието на повърхността потенциал може да повлияе на свързването на хидрофобна повърхност на мембраната и амфифилни мембранни проби йон-ционни. Това ви позволява да използвате някои от сондите като повърхност потенциални показатели. Фиг. 7.9 показва структурните формули на някои проби. За всички тези съединения, спектрален интензитета на сигнала може да се корелира с количеството на сонда, свързан към мембраната и, следователно, с потенциалната стойност на повърхността. Такива проби, използвани за изследване на много от зареден фосфолипид везикули
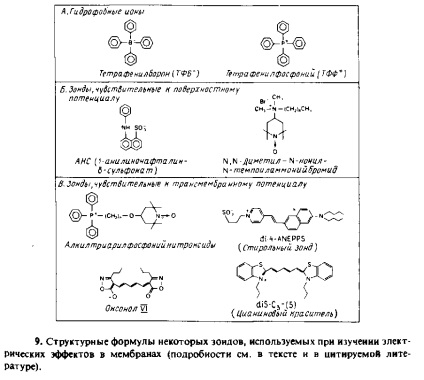
Изследване използването им Biomembranes-проблематично като спектралните характеристики на сондата може да зависи не само от потенциала на повърхността, но и от рН или потенциала на мембрана, което значително усложнява тълкуването на наблюдаваните спектралните промени. Като пример за ANS свързване с митохондрии и промяната на спектралните характеристики на неутрално червено при свързване към submitochondrial частици.
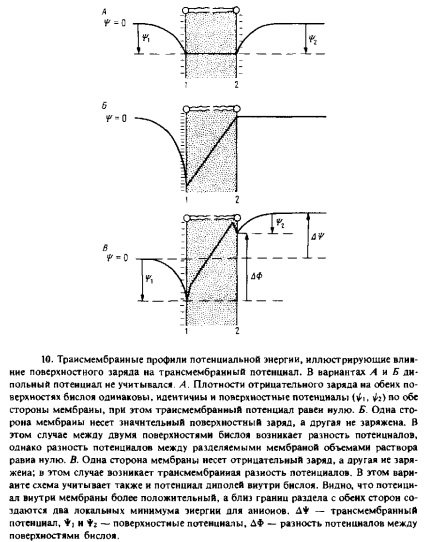
Фиг. 7.10, А показва профила на електрическия потенциал на мембрана, двете повърхности на които са отрицателно заредени. В присъствието на мембрана повърхностни потенциални увеличава в концентрацията на тази мембрана хидрофобни катиони като ТЕЦ + или К + -valinomitsin комплекс. Това се дължи на факта, че локалната концентрация на йони в близост до повърхността на мембраната е по-голяма от тяхната концентрация в по-голямата част. Припомнете си, че коефициентът на пропускливост могат да бъдат представени като продукт на коефициента на разпределение / 3 при постоянна скорост на движение на йони през мембраната на ИН поради големите количества / 3 отрицателно зареден мембранна пропускливост за хидрофобни катиони е по-висока от незаредени. Зависимостта на проводимостта на заряд мембрана повърхност е задоволително, описана от уравнение Gouy-Chapman за повърхностно потенциал.
Имайте предвид, че потенциалът на вътрешния диполи може да повлияе както на свързването на хидрофобни йони с повърхността на двуслойна и постоянна скорост на трансмембранен транспорт, докато ефектът на повърхността потенциал на симетричен пропускливост дължи изключително на неговия ефект върху коефициента на разпределение. В случая на асиметрична разпространение на повърхностни заряди, ситуацията се усложнява. Такива асиметрично разпределение на липиди - явление, по никакъв начин не рядко. В този случай, на ток през мембранния потенциал градиент да възпрепятства прехвърлянето на катиони от водната фаза 1 на фаза 2 и да се улесни прехвърлянето на катиони в обратна посока.
4. потенциал трансмембранен
трансмембранен потенциал е по дефиниция електрическата потенциална разлика между два водни фази отделя мембрана. Комуникацията между потенциал трансмембранния и потенциала на повърхността * аз и г ♦ графично показано на фиг. 7,10 А От диаграмата е видно, че потенциалната разлика между две повърхности DF мембраната може да се различава от L * резултат на разпределението на асиметричен заряд между двете повърхности на двоен слой. Всяка мембрана се намира вътре заредена група ще се движат в областта с потенциал DF. D * се нарича също потенциала покой и е тази стойност, ако е възможно, измерена двойка електроди.
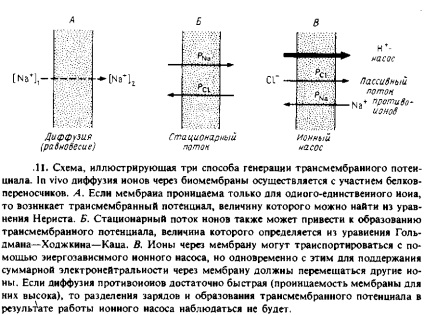
Създаване на трансмембранен потенциал по няколко начина. Схематично, те са изобразени на фиг. 7.11.
1. равновесни условия. Ако мембраната е пропусклива за всеки специфичен йонен като Na +. и непропусклив за други, след това може да бъде дифузионен потенциал която е пропорционална на логаритъма на съотношението на концентрациите на йони проникващи една и от другата страна на мембраната. Дифузията на йони през мембраната, последвано от разделяне трансмембранен заряд и по този начин създаде потенциална разлика предотвратява по-нататъшното разпространение. Таксата трябва да се премести през мембраната, за да създадете по тях с определена стойност ФАИ, може да се изчисли от капацитет на мембраната. За създаване на L * = 100 тУ трябва да се движат едно зареждане на 250 фосфолипидни молекули. Ясно е, че плътността на повърхностния заряд в същото време ще се промени много леко.
В равновесие, D * се определя от уравнението Нернст:
Същият уравнение може да се използва в случай на йон трансфер от валентността на Z. биомембрани пропускливост за йони, свързани с оперирането на специфични йонни канали. Тя може да бъде изкуствено увеличена чрез използване на специфични йонофори или йонни носители, такива като К + валил-nomitsina.
Стационарни дифузия йонен ток. Ако мембраната е пропусклива дял няколко йони, те ще се движат през него. В условия на стабилно състояние, поради разликите в проницаемост коефициенти за различни йони може да бъде трансмембранен потенциална разлика. С други думи, разделянето на зареждане в мембраната в такава ситуация би се дължи на факта, че някои йони дифундират през мембраната по-бързо от другата. Уравнението описва тази ситуация, наречена уравнението на Goldman-Hodgkin-Katz и в случай на две йони е както следва:
Движение на йони ще продължи дотогава, докато не се установи равновесие.
Активен транспорт на йони. разделяне трансмембранен заряд може да се наблюдава чрез активни транспортни процеси. Много ензими катализират реакция, свързана с пренос на заряд вектор чрез двоен слой. В Примери сортовете АТР-зависим йонни помпи, като Са2 + -ATPase активност или цитохром с оксидазна, която е на протонната помпа. Тук ние се отбележи, че само тези ензими катализират реакции са електрогенни, т. Е. са придружени от прехвърляне на такси чрез двоен слой. Очевидно е, че в такава система, трябва да има някакъв вид на неутрализиращи трансмембранния йонен поток. Системата е показано на фиг. 7.11, такъв поток е пасивна kontrtransport йон CI
Това се случва, когато на протонната помпа. Както в случая на пасивен йонен поток, брояч скоростта на потока ще бъде по-малка от скоростта на активното процеса, и в резултат на общия поток на йони чрез двоен слой няма да бъде електрически неутрален и мембранния потенциал разликата възниква №. Ако йони двуслойна пропускливост неутрализиращи да направят достатъчно големи, разделянето на зареждане ще бъдат унищожени. Този принцип се основава на използването на йонофореза за премахване на трансмембранния електрическия потенциал създаден като биологичните мембрани, а в моделни системи.
Свързани статии
