Еквивалентно на веществото се нарича сумата от него, който е свързан с един мол от водородни атоми или замества с химически взаимодействия.
Моларното масата на еквивалентен материал - маса от един еквивалент на веществото; Тя се изчислява като моларната маса на веществото, разделен на броя на еквивалент вещества.
Според закона еквиваленти вещества взаимодействат помежду си в количества, пропорционални на техните еквиваленти. Следователно, моларен еквивалент тегло на всяко вещество може да се намери, въз основа на взаимодействие с друго вещество, което е известно моларна маса еквивалент.
За тази лаборатория, трябва следните реактиви:
2. солна киселина HCl;
3. СаСО3 на калциев карбонат.
Въпроси за допускане до лабораторната работа:
1. Текстът на закона еквиваленти.
2. Какво е еквивалент?
3. Каква е еквивалентен брой?
4. Как да намерите еквивалентен брой прости вещество?
5. Как да намерите еквивалентен брой оксид?
6. Как да се намери еквивалентен брой хидроксид?
7. Как да намерите еквивалентен брой киселина?
8. Как да се намери еквивалентен брой сол?
Опитът №1. Определяне на моларен еквивалент тегло на алуминий
Реакциите се провеждат с отделяне на газ, моларната маса на веществото еквивалент могат да бъдат определени чрез обемно - освобождаване на газ от обема.
Методи за опит. Леярската тръба 5,6 мл разтвор на солна киселина солна киселина и поставени в алуминиеви тръби ръба Al претегля така, че металът не е в контакт с киселина. След свързване на флакона с устройството за определяне на обема на газ - тя се състои от две стъклени тръби, напълнени с вода, свързани помежду си чрез вида на скачените съдове. Като отбелязва нивото на водата в тръбата, която е свързана към тръбата, нулиране металната проба на киселината. Газообразният вещество освобождава по време на реакцията, и нивото на водата в тръбата, която тръба е свързана, се понижава. Когато нивото на водата в тръбата се стабилизира, довършителни опит.
По време на експеримента, на следния реакцията протича:
Запишете изходното изчисление dannyedlya алуминиев моларно еквивалентно тегло в следния модел:
Проба тегло - М, г;
Количеството освободен водород - V, мл;
Опитът Температура - т, ° С;
Атмосферно налягане - Р, mm Hg. Чл. ;
налягането на водната пара - Н, mm Hg. Чл.
Тук е обемът на еволюирал водород при нормални условия с формулата:
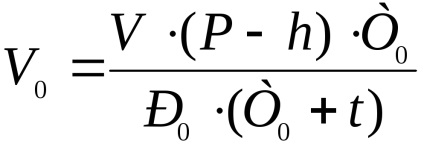
където V - обем на еволюира водород, мл;
P - атмосферно налягане, mm Hg.
т - температура тестове, ° С;
ч - налягането на водната пара при температурата на изпитването, мм живак;
T0 - температура, съответстваща на нормални условия, K;
P0 - налягане, съответстващо на нормални условия мм живачен стълб
Запишете обема на еволюирал Изчисляване на водород при нормални условия на горната формула, като се отчитат получените входни данни.
Ние очакваме алуминиев моларен еквивалент тегло при използване на формулата:
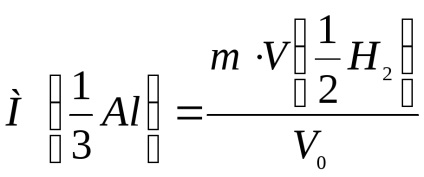
където m - маса на пробата, г;
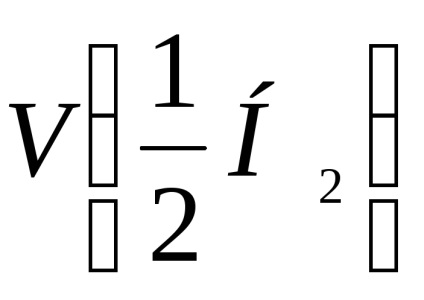
V0 - обем на водород разви по отношение на референтни условия мл.
Изчисляване Запишете алуминиев моларно еквивалентно тегло от горната формула.
Опитът относителна грешка изчислява по формулата:
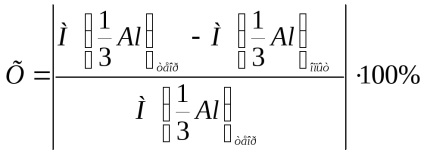
където
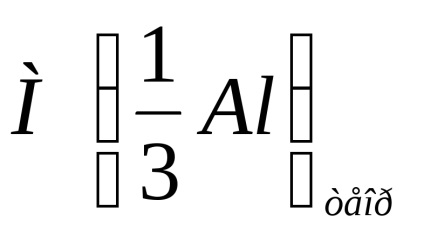
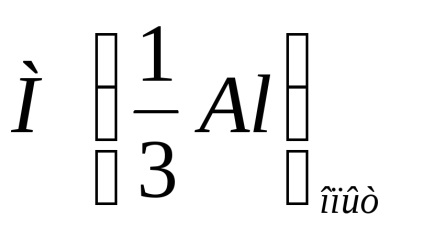
Запишете относителната изчисление грешка опит povysheukazannoy формула.
Направете извод за този метод на определяне на моларната маса на еквивалентно вещество и посочва до каква грешка беше установено в този случай.
Опитът №2. Определяне на моларната маса на еквивалента на калциев карбонат
Моларен еквивалент тегло на веществото може да се определя от броя на веществата взаимодейства с точно известно количество от друго вещество.
Методи за опит. Флаконът се поставя проба от мрамор (калциев карбонат СаСО3) и се добавя 4 мл (0,004 DM 3) HCl разтвор на солна киселина с моларен еквивалент концентрация от 0.5 мол / дм 3.
По време на експеримента, на следния реакцията протича:
След отделянето на газ престане, останалата част от мрамор промива, изсушава се и се претегля.
Ние очакваме тегло на калциев карбонат взаимодейства със солна киселина съгласно формулата:
където m1 - начално тегло на пробата в грамове;
m2 - крайното тегло на пробата, г
Запишете на изчисление на тегло калциев карбонат, нереагирал солна киселина, в горната формула.
Ние очакваме моларна маса калциев карбонат еквивалент на формулата:
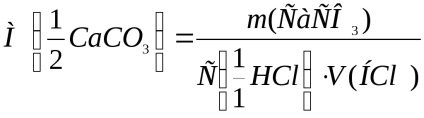
където m (СаСО3) - тегло на калциев карбонат взаимодейства със солна киселина, г;
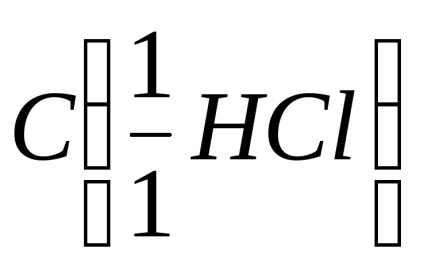
V (HCl) - обем на dm3 солна киселина.
Запишете изчисляването на моларно тегло на калциев карбонат еквивалент от горната формула.
Опитът относителна грешка изчислява по формулата:
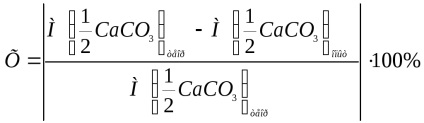
където
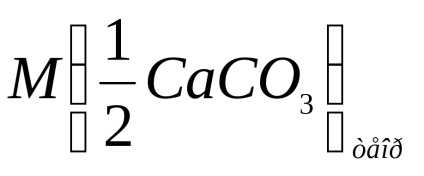
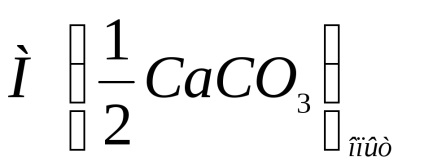
Запишете относителната изчисление грешка опит povysheukazannoy формула.
Направете извод за този метод на определяне на моларната маса на еквивалентно вещество и посочва до каква грешка беше установено в този случай.
Въпроси за защита на лабораторните упражнения:
1. Какво определя еквивалентен брой на химическо взаимодействие?
2. Как да намерите еквивалентен брой процес йонна размяна?
3. Как да намерите еквивалентен брой на редокс процес?
4. Какво е факторът на равностойност?
5. Как да се намери моларната маса на еквивалента на вещество?
6. Как да намерите моларната маса на еквивалента вещество, присъстващо в реакцията?
7. Как да се намери сумата на еквиваленти на веществата?
8. Как да се изчисли количеството моларни еквиваленти на газообразно вещество?
9. Какви са обеми ще се при нормални условия, еквивалент на един водород и един еквивалент от кислород?
1. NL Глинка. "Общото Chemistry". Ръководителят на "Еквивалентно. еквиваленти закон. "
2. EM Ribalkin, ОВ Kovalik. "Химия. Образователна визуална помощ. " Ръководителят на "еквивалентно".
3. RM Belkin VD Иванова. "Еквивалентно. Еквивалентното тегло. Прехвърляне с практическите уроци. "
Свързани статии
