чуваме доста често в обикновения живот, думата електролиза. Но не всеки знае какво означава това.
Електролиза - физико-химичен процес. По време на преминаването на които има постоянен електрически ток през електролита. В електролиза на положително зареден електрод има име - анода. А с отрицателен заряд - катод. Преместване частици, наречени йони в електролита. По време на процеса на електролиза положителни йони - -dvizhutsya катиони на катода, отрицателни йони - аниони - ход на анода.
Най-често в обикновения живот, думата означава електролиза на вода електролиза. Това е процес, при който вода с електрически ток се разлага на водород и кислород. И това е описан със следната химична реакция.
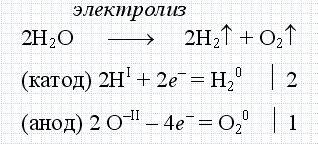
Процесът на електролиза е много широко използван в областта на науката и индустрията. Например, само чрез електролиза, алуминий се произвежда днес. Това е, следователно, това производство, поради високата цена на електроенергията.
Основните физични закони, които описват електролиза са Фарадей право.
През 1832, Фарадей установено, че тегло М на веществото, се разви в електрода е пряко пропорционална на заряд Q електрически, преминава през електролита:
ако електролитът се прекарва през време на време T с постоянен ток сила на настоящата I.
Коефициентът на пропорционалност
к се нарича електрохимичен еквивалент на веществото. Тя е числено равна на теглото на веществото, освободена по време на преминаването през електролита на единица електрически заряд, това зависи от химическата природа на веществото.
Този закон се нарича - Първият закон на Фарадей.
Вторият закон на Фарадей:
Ion химически еквивалент е отношението на моларното масата на своята валентност йон Z. Следователно, електрохимичната еквивалент.
Вторият закон на Фарадей е написано, както следва:
където
М - моларен маса на веществото се образува (но не е задължително да еволюира - и това може да започне във всяка реакция веднага след образуването) поради електролиза, г / мол;
I - ток интензитет преминава през вещество или вещество смес (разтвор, стопи), А;
т - време, през който електролиза се извършва с;
F - Фарадей константа Kd · мол-1;
п - номер на електрони, участващи в процеса, че при достатъчно големи стойности на ток, равен на абсолютната стойност на зареждане на йон (и противойонът), участва в електролизата (окислен или намалена). Все пак, това не винаги е така; например, медни соли в разтвора за електролиза (II) могат да бъдат получени не само свободната мед, но медни йони (I) (при ниска ток).
