Откритият урок на тема: "Историята на откриването на строежа на атома"
"Потърсете целия началото, и ще разберете повече." (Козма барове).
Вид на урока: урок учене на нови материали.
Цел: да се изследва структурата на атома.
- Изследване на планетарния модел на атома.
- За да се запознаят студентите с основната хипотеза на Thomson и Ръдърфорд.
- Разглеждане на историята на откриването на неутрона и създаването на модел на протонната неутронен на атома.
- Работни умения за определяне на състава на атома, атомно ядро състава на периодичната система на химичните елементи.
- Продължи развитието на умения в основната схема, таблици и диаграми.
- Разработване на интелектуални и творчески способности на учениците.
- Разработване монолози.
- Способността да се оформят собствената си работа с различни източници, обобщава материала в подготовката на проекти.
- Разработване на познавателния интерес към темите.
- Показване на стойността на опитните факти.
- Покажи ролята на важни учени в развитието на науката.
Оборудване: портрети на учени; периодичната таблица на химичните елементи Менделеев; филм "Rutherford" (фрагмент); образуват абстрактен препратка (за всеки ученик).
- Встъпителни думи от преподавателя, определяне на цели за уроците.
- Представянето на новия материал.
- Тестване на материала учи.
- Обобщавайки резултатите. Домашна работа.
Историята на физиката е една от най-интересните и очарователни страници - е историята на откриването на сложната структура на атома. В края на XIX- началото на ХХ век. идеи за строежа на атома е във въздуха, различни предположения на учените създадоха духовна атмосфера, в която в края на краищата, роден и откритие, тъй като тя не е била известна по това време нищо за вътрешната структура на атома. Целта на урока - турне през историята на виждания за строежа на атома, от древни времена до началото на 20 век, за да се запознаят с основните експерименти и теоретичната работа на края на 19 - началото на 20-ти век, които се обърнаха на концепцията на атома, и донесе да се създаде нов квантов модел на атома.
В началото на атомната структура поет Bryusov открития през 1922 г., пише прекрасно стихотворение "Електронен свят":
-Може би тези elektrony-
Светове, където пет континента,
Изкуство, знания, войни, тронове
И паметта на четиридесет века.
-Но може би един атомен
Вселената, сто планети,
Там всичко е компресирана в обем,
Но също така е нещо, което не е тук.
-Техните действия са малки, но все пак
Тяхната безкрайност, тъй като тук
Има скръб и страст, както тук, и дори,
Налице е една и съща арогантността на света.
Gipottza за съществуването на атома като неделими частици, различни конфигурации, които образуват празнотата заобикалящия ни е обективния свят, е толкова стара, колкото нашата цивилизация. Концепцията на атома е на ръба на най-слабо нейните 25 века.
Демокрит (460 -. 370 години преди новата ера) - дойде от богатите и известните сланината в Северна Гърция. Всички наследени пари той прекарва по време на пътуването, където е придобил задълбочени знания. Жителите на града го разпознава като градински чай.
Демокрит е убеден atomist. Основните елементи на картините му на природата са както следва:
- всички органи се състои от атоми, които са неделими и неизменна форма;
- броят на атомите е безкрайна, броят на различните видове атоми е безкрайно;
-атоми имат различни издатини, вдлъбнатини, куки, което им позволява да се образуват стабилни съединения;
-атомите са в постоянно движение.
-Ето един поглед: Когато слънчева светлина прониква
-В домовете ни и намалява мрака със своите лъчи,
-Много малки тела във вакуум, ще видите трептене
- Прибързаното насам-натам в завладяващия блясък на светлината;
-Като че ли в една вечна борба те се бият в битки и сражения
-В битките хвърлени изведнъж по заповед, а не знае покой.
-Може ли да се изясни това, за да се види как безмилостно
-Ultimate начало на нещата в по-голямата празнота размах.
В България, на теорията за най-малките частици на материята, разработен Михаил VasilevichLomonosov. Разграничаването между два вида частици материя, като им дава името "елементи" - атоми и "телца" - молекули.
"Елемент е част от тялото. Тя не се състои от всяка друга частица, и "телце" е колекция от елементи в една голяма маса "
Така че това беше предложено на молекулата се състои от атоми.
Въпреки това, до края на 19 век, има неоспорими факти, които сочат към сложната структура на атома. Най-сериозният удар към познатия концепцията на атома, причинено откриването на електрона - частици, част от атома и последва след първия опит да се създаде модел на атома.
Така Джоузеф Джон Томсън
Проектът е Влад Смоленск
Student. Прави се съобщава атомен модел, предложен от британския физик JJ Thomson: .. "Atom" на гръцки - неделими. Но след откриването на електрона през 1897 г. и е част от атома, заключението за сложната структура на атома е направено. Първо развита достатъчно на модел на атома е предложен от английски физик Джон. Джон. Томсън открива електрона. Според този модел вещество в атом носи положителен заряд и равномерно изпълва целия обем на атома. Електроните са "вградени" в атома. Приема се, че много от тях. Като цяло elektroneytrallen атом. За стабилност атоми необходимо електроните разположени в концентрични слоя, всеки слой на определен брой електрони. Thomson се използва моделът, обясни редица физични явления. Например, една добра проводимост на метали се дължи на факта, че металните атоми лесно губят някои от електрони.
Първият атомен модел играе положителна роля, впоследствие се използва вярно идея на електроните в слоеве атом, загубата на електрони от атоми. Въпреки това, скоро открих модела несъответствие на реалността. По-специално, моделът на коледен пудинг е в противоречие с резултатите от опита на Ръдърфорд. "
Въпреки това, веднага след това откри противоречие на този модел всъщност атом. По-специално, моделът на коледен пудинг е в противоречие с резултатите от експериментите на Ърнест Ръдърфорд - един от основателите на атомната и ядрената физика, член на Кралското дружество, почетен член на 30 академии и научни дружества, включително и на Академията на науките SSSR.V 1908 - Нобелова награда за проучване на радиоактивност. учениците Му бяха Чадуик, Бор, Пьотър Капица.
Пьотър Капица пише: "Аз не мога да мисля за друг съвременен учен Ръдърфорд, в лабораторията, които са довели до много видни физици. Историята на науката показва, че на великия учен - не е задължително един голям човек, но велик учител не може да бъде чудесен човек "!
Проектът е Ivanochkin Анна
Student. Това прави обяснения на планетарния модел на атома, в резултат от експериментите E.Rezerforda. През 1909 г. - 1911 години. Rutherford експериментално доказано, че атомите имат ядра. През май 1911 г. в страниците на лондонския "Философски Magazine", той очерта резултатите от експерименталната и теоретична проучване в областта на атомната структура. Ядрото заема малка част от обема на атома, е положително заредена и се концентрира почти всички атомната маса, тъй като електроните в сравнение с атома много леки частици. Електроните се движат около ядрото.
Частиците на алфа от радиоактивен източник, преминаващи през отвора да паднат върху тънък фолио злато. Той има дебелина от около един микрон, т.е. Тя се състои от около 3000 атомни слоеве. Повечето от частиците на алфа може лесно да премине през фолиото, се отклонява малко. Но някои редки алфа частици се отклоняват при големи ъгли и дори при ъгли, близки до 180 °, т.е. почука обратно.
Резултатите от тестовете могат да бъдат обяснени, както следва. Алфа-частици, преминаващи през фолиото, преминават през златните атоми. Това е възможно, тъй като светлината електрони имат почти никакво влияние върху движението на тежкотоварни алфа-частици. Тъй като в повечето случаи те се отклоняват от малки ъгли, атомите в повечето от обема си, пълни с електрони, и само малка част от тях се положително зареден материал. Тази централна част на атома се нарича ядро. От експерименти, които ядрото и избутва алфа частица, която е по-силна, колкото по-близо до ядрото преминава. От съотношението между общия брой частици и броя на отхвърлено при определени ъгли изчислява размера на частиците на ядрото и ядрен заряд. Установено е, че основната радиус от порядъка на 10 - 12 cm (10-14 м). Зареждането на ядрото е положителен и определен от формула Q = Z • д, където Z - пореден номер на елемента в периодичната таблица и Е модула електронен заряд.
1 Може би тези elektrony-
Светове, където пет континента,
Изкуство, знания, войни, тронове
И паметта на четиридесет века.
2 Друг, може би всеки атом -
Вселената, сто планети,
Има всичко тук, сгъстен до такава степен,
Но също така е нещо, което не е тук.
3 Тези мерки са малки, но все пак
Тяхната безкрайност, както тук,
Има скръб и страст, както тук, а дори и
Налице е един и същ свят арогантността
4 Техните мъдреци, тяхната безгранична свят
Поставянето на центъра на съществуване,
Побързайте да проникне в тайните на искрата
И umstvuyut как сега
5 А в момента, когато унищожаването на
Хепънинг по отношение на нови сили.
Cry в сънищата на самовнушение.
Това Бог фенерчето потушен!
Терминът "неутрон" се появява много по-рано откритие на самата частица. Тя се отнася до един вид неутрална структура на материята. Идеята за съществуването на неутрона във въздуха и никой не знаеше какво облик той трябва да вземе.
Джеймс Chedvikpoluchil Нобелова награда за своя "откритие на неутрона"
Неговият проект е Дмитрий Fedosov
Откриването на неутрона - ключът към ядрената физика. Делене на урановите ядра с неутрони "невероятно" и "зловеща" откритие.
Значение отваряне атом изследват Veligodskaya Дара и дружина Дария
И в заключение искам да ви чете стихотворение, което е писано от ученик на клас 10 Shulpina Дария
Домашна работа по физика: § 94. Работа у дома с учебник, попълнете статията се отбелязва. Ние предлагаме деца по искане на една творческа задача (написана на дъската):
Направи си измислиш история във всеки жанр (приказки, басни, детектив, и т.н.): Какво мислите, прилича на един атом?

История на откриването на строежа на атома

Демокрит (460-370 г. пр.н.е.)

Основните елементи на неговата теория на атомната структура
- Всички органи са съставени от атоми, които са неразделна част и фиксирана форма
- Броят на атомите е безкрайна
- Атомите имат различни изпъкналости, канали, куки, които им позволяват да образуват стабилни съединения
- Атомите са в постоянно движение

"Елементът е част от тялото, състояща се от не по-малки количества от други частици" и "телце е колекция от елементи в малка маса."

Модел "слива" атом

Математик въпрос за физика
- Проучвахме преминаването на електрически ток през изредените газове
- Отворен (1897), на електрона и се определя (1898), заряда
- Той предположи, (1903), един от първите модели на атома
- Електрическият ток в изредените газове
- Той обясни, непрекъснатост на спектъра на рентгенови лъчи
- Аз изложи идеята за съществуването на изотопи и получи своята експериментална проверка
- Един от създателите на електронната теория на металите

- През 1882 г. получава наградата Адамс за работата си по предложение на вихри
- През 1897 г. той открива електрона, за която през 1906 г. е удостоен с Нобелова награда по физика с текста "за изучаване на преминаването на ток през газове."
- Той е удостоен с медал на Бенджамин Франклин (1923), М. Фарадей (1938), Копли (1914) и други.

Започва методическото проучване на количественото отклонение на катодните лъчи в електрически и магнитни полета. В опита Thomson доказано, че всички частици, образуващи катодни лъчи са идентични една на друга и са част от веществото.
Същността на експеримента е хипотезата за съществуването на материята в състояние на още по-фино раздробяване от атома.
Тези частици, които са били част от лъча катод са малко, наречени електрони.
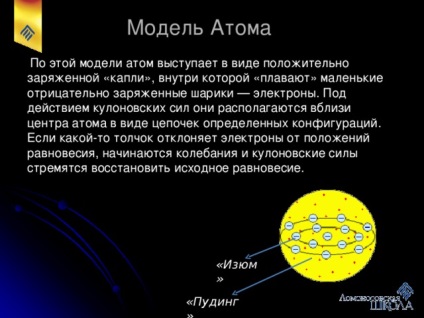
Според този модел атом действа като положително заредени "капки", в който "флоат" малки отрицателно заредени капчици - електрони. Под действието на силите Кулон, те са разположени в близост до центъра на атома на верига специфични конфигурации. Ако тласък отклонява електроните от своите равновесни положения, като се започне колебание и Кулон сили са склонни да се възстанови оригиналния баланс.

Основните идеи на Thomson
- На слоевете на електрони в атома
- Загубата на електрони от атоми
- На стабилността на атома

"Не мога да мисля за друг съвременен учен Ръдърфорд, който е израснал в лабораторията са били толкова много видни физици"

структурно атома

Свързани статии
