Проблеми с решението. Термодинамиката.
1) идеален газ, чиято маса m и молекулна маса μ. zobarno разширява в определено налягане. Основно температура газ Т1. 2. Определяне на окончателната T работата, извършена от газа.
Решение.
Работа в изобарен процес
От уравнение Менделеев-Клапейрон
Оказа се, че работата в изобарен процес може да се изрази не само от промяната в обема в съответствие с формулата, но и чрез промяна на температурата: зало-
получен резултат трябва да се има предвид, тъй като той често се използва за решаване на по-сложни проблеми.
отговори на:
2) хелий (He) се нагрява при постоянно налягане. По този начин той съобщи, Q = 20 кДж на топлина. Определяне на промяната във вътрешната енергия на газа и усъвършенства своята работа.
Решение.
Тъй като състоянието на проблем р = CONST. газът работи където m - маса на газ, ц - неговата молекулна маса, # 8710; Т - е промяна на температурата.
Хелий - едноатомен газ, така че вътрешната си енергия и вариант Сравнявайки формули А и за промени в вътрешен енергиен # 8710; U. получи, че пиша първия закон на термодинамиката за този процес:
Затова работата на промяна във вътрешната енергия
отговори на:
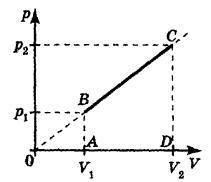
3) температурата на масата m на идеален газ с моларна маса μ варира като където а = конст> 0. Виж работата, извършена от нарастващия обем на газ от V1 към V2. топлина в този процес се абсорбира или освобождава?
решение:
Процесът не е нито изобарен или изохорен, много по-изотермичен. Re Cording BR ядат за всяко състояние в процеса на Менделеев-Clapeyron уравнение: От тогава след заместване ние получаваме зависимостта на налягането от обема на диаграма на тази функция е показано на фигура.
Перфектна работа на газ
За да се отговори на втория въпрос, задачата ще използва първия закон на термодинамиката: Тъй като газът се разширява, тя работи A> 0. Промяната на вътрешната енергия на идеален газ е пропорционално на промяна на температурата: # 8710; U
# 8710; И T. Тъй като увеличава обема, температурата се повишава и следователно # 8710; U> 0. След това, и Q> 0, което съответства на топлина абсорбция на газа.
4) Когато адиабатно компресиране на 1 мол едноатомен газ е направена от външни сили работа A. колко пъти повишени средноквадратична скорост на молекулите на газа, ако началната температура на газа е Т 1?
Решение.
Първият закон на термодинамиката на адиабатно процес се записва като 0 = # 8710; U + A ". където # 8710; Най-U - промяната на вътрешната енергия на газа, A '- работи на газ в този процес. Тъй като газът се пресова, след което А '<0. в то же время внешние силы совершают положительную работу А, причем А' = -А. Следовательно, Внутренняя энергия 1 моля идеального одноатомного газа поэтому . Отсюда выражаем конечную температуру газа
Средната кинетичната енергия на молекулите където Т - температура. Тогава средната квадратна скоростта
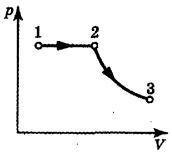
решение:
Построява се графика на натиск от обхвата на оси р, V (фигура): 1-2 - изобарно нагряване, последвано от увеличение на обема; 2-3 - адиабатно разширение. Работа в адиабатен процес
защото
Ето защо,
Количеството топлина, произведено в изобарен процес газ:
Заместването от уравнение (1) температурната разлика установи, че
отговори на:

6) тегло М на идеален газ при температура T. изохорен охлажда, така че налягането пада до п пъти. След това газът се разширява при постоянно налягане. В последната държава, нейната температура е равна на оригинала. молекулна маса газ ц на. Определете най-перфектната работа на газ.
Решение.
Г-н Рафик този процес е показано на фигурата. Ето 1-2 - isochore 2-3 - isobars. Любими работа, където А1 _2 - Работата в областта 1-2 и А2-3 - Работата в областта 2-3. На гарата 1-2 V - Конст. обаче A1-2 = 0. част 2-3 р = конст и изразяване на този тип трансформират, така че да се извлече продуктът от налягането в обема в състоянието, в което зададената температура:
От уравнение Менделеев-Клапейрон за държавна 3, откриваме, че
Тъй като от състояние 1 до състояние 3 може да се движи по протежение на изотермите на 1-3 (в този случай ние казваме, че точките 1 и 3 са разположени на една и съща изотерма). Според закона на Бойл
След настройка във формулата (1), получаваме
отговори на:
1,484,303 уникални посещения
Свързани статии
