Ентропия и вероятност на държавата
Известно е, че всяка система, без излагане на външната тенденция да влезе в състояние се характеризира с минимум потенциалната му енергия. Тази информация позволява известна степен се предвиди посоката на потока на процеса ин виво ", без ефект върху тялото или системата отвън Освен това, както е показано на Клаузиус, реални процеси винаги се развиват по такъв начин, че един от най-важните характеристики на състоянието на системата -. Ентропията - увеличаване на . Ето защо, всяка термодинамична система ще се развива в посока на потенциалния минимум на енергия и максимална ентропия. Но не само потенциална енергия и ентропията може да помогне при определянето посока на потока на реални процеси. Има и друг, статистическа, природен закон, който гласи, че най-вероятно е държавата с най-голямо разстройство.
Помислете за един плавателен съд, съставен от няколко свързани помежду си клетки. Сложете в н молекулите на кръвоносните съдове, които могат да се движат свободно на кораба от клетка в клетка, които са разпределени както пожелаете. Естеството на това разпределение може да бъде доста разнообразна. Като пример, помисли за разпределението на шест молекули в съда от трите клетки. Прости аргументи, за да ни убеди, че може да има различни начини за разпространение на молекули в клетките, някои от които са показани на фигура 9. Например да разгледаме следната ситуация. Кутията се разделя на дялове в три отделения. Нека един от тях в молекулата; Две други - са празни. Тя може да се разглежда като такава система за частица нареди. Сваляне на преграда между отделенията, ние отбелязваме, че молекулите, които участват в хаотично топлинно движение, след известно време ще отнеме цялата сума, предвидена за тях. Наблюдавайки допълнително, ние виждаме, че молекулите са преразпределени така че всяко от отделенията съдържат приблизително същия брой молекули, въпреки че някои вариации са неизбежни и - колебания, които ще бъдат по-малка, толкова по-голям първоначален брой молекули в кутия. По този начин, системата е оставена сама на себе, става дума за най-вероятното състояние: еднакъв брой молекули в всяко отделение. Този процес преразпределение се развива в посока, след което се увеличава ентропията; и системата въпрос за най-вероятната държавата. В противен случай, увеличението на ентропията е свързано с повишена вероятност състояние. Количественият характеристика на вероятностите на щатите е термодинамична вероятност, което е нищо друго, освен броя на начините, по които могат да бъдат реализирани на състоянието на физическата система. Разпределение съответстващ на фигура 9, е най-вероятно.
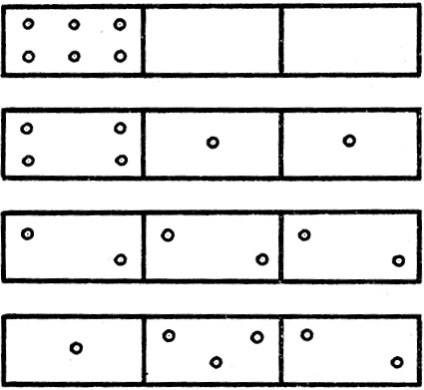
Фиг. 9. Методите за молекулно разпределение на клетки
С изучаването на термодинамичните процеси Болцман забелязал сходство в промените посоката на ентропията на системата и на стойност от термодинамичната вероятността от държавата. Той открива, че ентропията на термодинамична система е пропорционална на логаритъма на вероятността за своето състояние. Повишена ентропия означава поръчка нарушение, аспирационната система за произволно движение на частиците, изграждащи го. Според теоретични изследвания на Болцман
Съгласно теоретични изследвания Boltzmann (34)
където S - ентропия на системата; W - термодинамична вероятност му състояние.
Разработване на по-нататъшни идеи на Болцман за връзката между ентропия и вероятност на държавата, на немския физик Макс Планк намери фактор пропорционалност в (34) и получи равен
Коефициентът на пропорционалност (35)
където к - константа, по-късно наречена константа на Болцман.
От работата на Болцман и Планк това следва, че втория закон на термодинамиката, както и първата, е закон за статистиката. Вторият закон на термодинамиката е вярно само за голям брой молекули, към които можете да приложите статистически методи. Създадена увеличение Клаузиус ентропия трябва да се разбира като средна мощност. В някои части на процесите на системата може да се развива по такъв начин, че ентропията на тази част от системата може да се намали, въпреки че като цяло macrosystem се характеризира с увеличаване на ентропията. Тези колебания в плътността на енергията, температурата непрекъснато се появяват и изчезват в относително кратки интервали от време. Най-вероятно държавата означава, че системата е в състояние на термодинамично равновесие. Връзката между ентропията и термодинамичната вероятността предполага, че ентропията е мярка за близост на изолирана система за термодинамично равновесие.
Свързани статии
