дефиниция
рН се определя като отрицателен логаритъм на водороден йон активност, А +, в rastvore.Takim начин: рН = - дневник (А +)
рН технологии Измерване
рН се измерва с помощта на апарата на два електрода: измервателен електрод и сравнителен електрод. Тези два електрода често са комбинирани в един, който се нарича "комбинация електрод." Всички рН електроди доставени FLS, са "комбинирани".
Когато два електрода се потапят в разтвора, електрохимичната клетка се образува малък. Разработеният потенциал зависи от двата електрода.
Измерената напрежение може да бъде изразена чрез уравнението Нернст както следва:
Е = Emeas - EREF = Е0 - (2,303RT / F) рН където
Е = измерено напрежение
Emeas = измервателния електрод
Напрежение EREF = сравнителен електрод
Е0 = стандартната потенциал електрод
R = постоянен газ
T = абсолютна температура
F = Фарадей постоянна
Освен това, това означава, че връзката между рН и Е са линейно свързана с температура.
Наклон стойност при + 25 ° С е 59.18 тУ / рН. Това е около 54 тУ / рН при + 5 ° С и около 62 тУ / рН при + 40 ° С В + 100 ° С стръмността увеличава до приблизително 74 тУ / рН.
Технически термини рН
Определяне на отклонението, а наклонът на кривата на рН на системата.
За оценка на характеристиките на двете калибриране електроди трябва да се извършва за двете точки на рН.
разтвор за калибриране проба може да се проведе за изследване на химически вещества, които могат да повлияят на измерването на рН.
калибрационен разтвор (буфер течност)
А разтвор с известна стойност на рН, се използват за рН калибриране система.
В калибрационните разтвори, засегнати от температура.
Зависимостта на температурата на буфер течност е добре известно.
След това, посочва зависимостта на буфер течност доставени FLS:
За сравнение, показатели рН често корелира с определена температура, обикновено 25 ° С
автоматична компенсация на температурата
Алгоритми за автоматично преобразуване на рН на проба за контрол на температурата.
Тази функция се вземат предвид промените в кривата на рН в сравнение с температурата.
Операционната принципа на рН-електрод
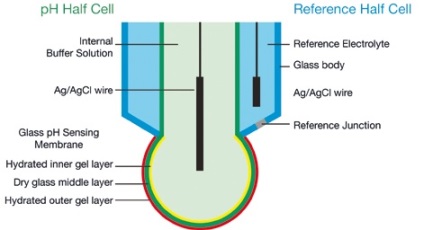
рН-електрод е много висок импеданс електрохимична клетка, в която потенциала образуван между рН полу-клетка и референтната половината клетката е сумата от различни потенциали. Фигура А показва типична комбиниран стъкло рН-електрод, при което рН-половин клетката и референтната половината клетка са комбинирани в една структура.
В идеалния случай, всички потенциали са постоянни, с изключение на един, генерирани на външния слой на хидратиран гела, която зависи от рН-сонда, в съответствие с уравнението Нернст.
Real електроди се различават от идеалния електрод поради различни фактори, включително:
1) производствени допуски;
2) стареене на електрода;
3) събиране и пречистване на електрода.
Всички m рН позволяват калибриране или стандартизация на електрод за компенсиране на споменатите по-горе ефекти. Стандартно калибриране включва измерване на отговор на електрода в две рН буфери с известни стойности на рН, и създаване на линейни карти отговор електрод за тези две точки. Тези резултати като отклонение коригиращи коефициенти и стръмността на кривата, когато отклонението е картографиране на тУ при рН 7 и стръмността на кривата е промяната в отговор на единица тУ рН, обикновено се изразява в тУ / рН, представляват процентът на кривата на идеален наклон електрод (59,16 тУ / рН при 25 ° С).
ORP
дефиниция
редокси потенциал (ORP) е мярка тенденция на разтвора за окисление или дезоксидация, че може да бъде в контакт с него.
Разтвор на окислител е течност, с тенденция към получаване на електроди, окисление, които в контакт с тях, се деоксидирането.
Деоксидирането разтвор е течност, с тенденция да губят електроди деоксидирането че в контакт с тях, се окисляване.
технологии за измерване ORP
ORP електрод произвежда напрежение, както и рН-електрод. В този случай, измерването се влияе не само от водородни йони, но също така и всички химически вещества, които могат да дадат или получават електрони.
Въпреки ORP влияе от температурата и, по принцип, трябва да бъде уравнението Нернст, е трудно да се компенсира за измерване, тъй като обикновено не е известно колко електрони участват в реакциите Redox (когато измерване ORP се използва само за наблюдение на реакцията може да се определи корен участва половината реакция и поради това може да бъде направя).
Измерването на ORP се използва и за инсталиране на два електрода: измервателен електрод и сравнителен електрод. Тези два електрода често са комбинирани в един, който се нарича "комбинация електрод." Всички ORP електроди се доставят от FLS, са "комбинирани". Когато два електрода се потапят в разтвора, електрохимичната клетка се образува малък.
Разработеният потенциал зависи от двата електрода и обикновено варира от -1000 тУ до 1000 мВ.
Въпреки това измерване не е свързан с конкретен течност може да бъде много полезна за наблюдение и контрол на активността на някои съединения. На практика, използването на наблюдение и контрол на окислително-дезоксидация реакции, използвани за унищожаване на цианид, дехлориране, нитрит и сулфит окисление, дезоксидация хромат, хипохлорит избелване, и също така за контрол на скрубери хлорен диоксид и хлор използване бисулфит ORP. измерване на концентрацията на АФП проблематично, но ORP може да се използва в някои случаи за откриване на течове, за да се определи присъствието на окислител или дезоксидатор.
Накрая, в някои случаи, ORP се измерва за контролиране на биологичен растеж на микроорганизми. Принципът на това приложение е, че минималната стойност на ORP микроорганизми са успешно унищожени. Този подход се използва при хлориране на басейни и охладителни кули. Трябва да се отбележи, че и в двете от тези приложения е провел и регулиране на рН.
Технически условия АФП
Определяне на аномалии редокс система.
За повечето приложения, ORP абсолютната точност е по-малко важно от скоростта и относителните се променя в системата. За много желани стойности на ORP изисква процедури и спецификации с допустимо отклонение ± 25 тУ и ± 50 тУ, или идентифициране на промените в ORP, например, капка 400 тУ, крайната стойност. Тъй като индикатор се използва в най-различни случаи на АФП със собствени специализирани методи за четене на необходимата производителност или промени в показателите, въз основа на опита, ние не може да се развива техниката в детайли. Достатъчно е да се каже, че точността, необходима за измерване на рН и други електрохимични измервания не са обикновено се използва за ORP, така калибриране ORP електроди и м не е толкова често.
Разтвор с известна стойност на ORP използва за проверка BDN система.
Както е обяснено по-горе, абсолютната стойност на ORP не е толкова важно, така ORP калибриране разтвор може да се използва само за целите на проверката.
По принцип калибриране разтвор или контролен разтвор ORP е предназначена само за да се улесни сравнението.
С други думи, отклонение оценка може да бъде задължително в случай на смяна на електрода, при пристигането на нов сензор измерва различна стойност от предходната електрод, обаче, калибриране може да се изисква да се провери новата стойност с предишната. Например, ако процедурата изисква желаната стойност от 410 тУ определя чрез използване предходната електрод и устройството, индикация на нов електрод със същия инструмент може да създаде 425 тУ в същата течност. Използването на калибрирането или, по-точно, отклонението за настройка може да се премахне разликата от 15 мВ, за да се избегне объркване. След това, когато четете следните показания те могат да бъдат лесно в сравнение с предходните показания електрода.
Операционната принципа на електрод ORP
Принципът на измерване е да се използва ORP електрод на инертен метал (платина, злато понякога, рядко сребро), които поради неговата ниска устойчивост ще дари електрони към окислителя или приема електрони от дезоксидатор. ORP електрод ще продължи да приеме или да дарят електрони, като развитие се дължи на натрупване на заряд равен разтвор АФП. Обикновено, точността на измерване ORP е ± 5mV. Също ORP електрод изисква сравнителен електрод, която обикновено е същата електрод на сребърни хлорид, който се използва за измерване на рН.
проводимост
дефиниция
Проводимост е способността на решение за провеждане на електрически ток. В настоящите решения понася катиони и аниони.
Способността на решение за провеждане на електроенергия зависи от няколко фактора:
- концентрация
- движението на йоните
- валентността на йони
- температура
Всички вещества са с различна степен на проводимост. Във воден разтвор ниво на йонна сила варира от ниска проводимост на ултрачиста вода високата проводимост на концентрирани химически проби.
технология за измерване на проводимостта
Проводимост може да бъде измерена чрез прилагане на електрически ток (I) към двата електрода, потопени в разтвора, и измерване на полученото напрежение (V). В процеса, катиони мигрират към отрицателния електрод и анионите - към положителния електрод и разтворът действа като проводник на електричество.
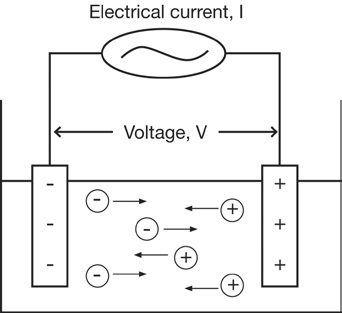
Съпротивлението на разтвора може да се изчисли (R), с помощта на закона на Ом
(V = R х I).
R = V / I
когато:
V = напрежение (волта)
I = ток (усилватели)
Разтвор R = съпротивление (ома)
Проводимостта (G) се определя като реципрочен на електрическото съпротивление (R) на разтвора между два електрода.
В действителност, кондуктометър измерва електропроводимостта и показва четенето превръща в проводимост.
Тази връзка между разстоянието (г) между електродите и областта (а) от електроди.
К = г / а
K = константа елемент (cm-1)
а = областта ефективното електрод (cm2)
г = разстояние между електродите (см)
Електричеството е поток от електрони. Това означава, че в разтвор на йони ще провежда електричество. Проводимостта на решение е възможността за провеждане на ток. Показания примерни промени проводимост в зависимост от температурата.
C = G х К
С = проводимост (S / cm)
G = проводимост (S), където G = 1 / R
K = константа елемент (cm-1)
Той е реципрочен на стойността на проводимостта, която се измерва в ома • см. Обикновено, той се ограничава до измерването на чиста вода, чийто проводимост е много ниска.
За да се определи необходимостта от постоянен елемент за преобразуване на показанията при провеждането на резултатите електропроводимостта.
А разтвор с известна стойност проводимост се използва за калибриране на проводимостта на системата.
За сравнение, проценти проводникова често корелира с определена температура, обикновено + 18 ° С, + 20 ° С или 25 ° С
автоматична компенсация на температурата
Алгоритми за автоматично преобразуване на температурата на пробата контрол проводимост.
Коефициент на компенсация на температурата
Фактор използва за автоматична компенсация. Обикновено, изразена в% / ° С
За използване с ултрачиста вода (UPW) с измервателни устройства FLS има специален корелация, базирани на ASTM D1125-19.
цялото разтворено твърдо вещество (TDS)
Това измерване е общата концентрация на йонни вещества в пробата.
Инструментът се калибрира съгласно стандартен разтвор или физиологичен разтвор, които потребителят реши да се използва като контролна проба.
Проводимост отчитания се превръщат в TDS показания на известни математически коефициент за умножение. Коефициентът зависи от контролния състав (обикновено физиологичен разтвор) се използва за получаване на стандартна или контрол материал. Например: морската вода съдържа много различни соли, а основно NaCl, така че потребителят да може да се съпоставят само с него. Ето някои примери за фактори:
коефициент на трансформация гама
Технически условия за проводимост
тороидални индуктивно устройство за измерване на проводимостта
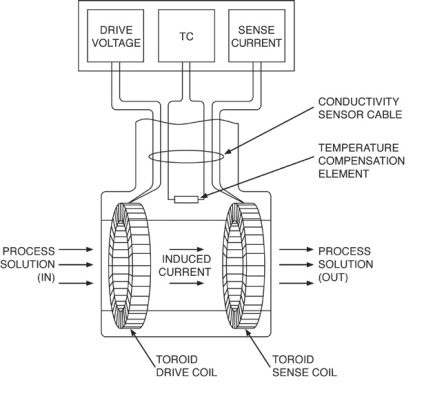
Индуктивен тороидални сензор проводимост се състои от две големи тороиди (бобини) концентрично и съседни един на друг, вграден в непроводящ жилища. първичната намотка е развълнуван от синусоидално напрежение, което създава променливо магнитно поле. Това променливо магнитно поле предизвиква йони в разтвора да пътуват през центъра на тороида. Движението на йони е еквивалентно на променлив ток, минаваща през центъра на тороида. ток променлив произвежда променлив ток в измервателната намотка, която е пропорционална на проводимостта на разтвора. В идеалния случай, сигналът в измервателната намотка трябва да се обуславя само чрез преместване йони и не с променливо магнитно поле, генерирани от първичната намотка. Поради тази причина, между бобините се нуждае от добър магнитен ekranirvanie.
изтегляне на PDF
Създаване на сайт "Актив"
Свързани статии
