Тези правила са полезни в много случаи. Виж, например, в може да бъде лесно определено чрез тяхното окисление променлив елемент (или неизвестни) валентност молекулна формула. Да приемем, че има връзка H2 SO3. Въпросът е, какво е степента на окисление на сяра? Тъй като степента на окисление на водород винаги (1), и степента на окисление на кислород (-2), че е лесно да се изчисли, че положителен и отрицателен окисляване степен "баланс" взаимно в молекула Н2 SO3, когато степента на окисление на сярата е (4). В този случай, алгебрични сумата от всички степени на окисление в молекулата е равна на нула:
Действието на това правило може да бъде показано с примера на реакцията на сяра с кислород, в който се движат електрони формално от един атом на друг:
Преди кислород реакция и сяра, имат същото - състояние нула окисление. Реакцията се увеличи степента на окисление на сярата (4). Следователно, серни оксиди.
Степента на окисление намален кислород (-2), т.е. кислород възстановява. Алгебрични сумата от всички степени на окисление в SO2 остава нула.
Подобни реакции със степента на окисление на реагиращите атоми - голям набор. Заедно те се наричат окислително-редукционни реакции.
В следващите глави ще разгледаме тези отговори в детайли, и все пак ще разберем в новите условия.
Точно както е трудно да си спомни какво процеса - или откат улавяне на електрони - нарича окисление, и които - възстановяване. Какво атом става отрицателен, а някои - положително окисление.
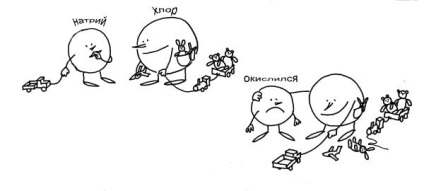
Фиг. 3-11. Не съвсем обикновено реакционната уравнение след химически: Na + Cl = NaCl (виж текста.). Хлор - "отрицателна", той избира други електрони. Натриев "окисляват" - е очевидно в кисел му лице.
За някои от вас ще разбера. 3-11, което говори за реакцията между натрий и хлор, като ако това се случи в "химична градина." Тази "детски" поръчки са същите, както в конвенционалното. Хлор играчки, колкото 7 (електрони). Натриев същото имам само камион (1 електрон). Хлор след това видях един камион Натриев и реши, че това е тази играчка и това не е достатъчно! Хлорът е по-силен, така че камионът моментално се обърна от него. И за да не доносник Натрий (той има вид на оксиди!), Хлор предложи да играят заедно. Какво е там! Разбира се, всички 8 играчки Хлор дръпна по-близо до него, и натриев остава само, че стои в непосредствена близост до "окисляват" изглед.
Така че, това, което е морално? Хлор, разбира се, отрицателен. Той взе играчка-електрон на някой друг. Сега той има отрицателно състояние окисление. Натрият се окислява със сигурност - която спечели него "кисел" външен вид. Но хлор не се отклонява - някои играчки са не повече! Какво не е снимка на образуването на химична връзка в типичен окислително-редукционна реакция?
Остава само да добавя, че в такива реакции се намалява окислител. и окисляват - редуктор. В нашата история, хлор - окислител, и натриев - редуктор.
Свързани статии
